题目内容
【题目】某化学学习小组欲探究己烷的性质,用己烷进行下列实验:
实验1:
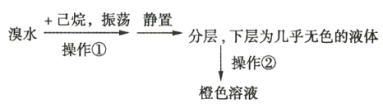
实验2:将上述橙色溶液装入密封性好的无色试剂瓶中。过一段时间,溶液颜色变浅,打开瓶盖瓶口出现白雾。
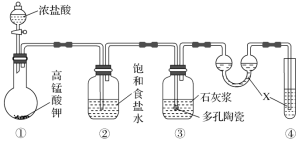
实验3:利用如图所示实验装置在一定条件分解己烷(生成丙烷和丙烯![]() ),且丙烯能被酸性
),且丙烯能被酸性![]() 溶液氧化。
溶液氧化。

(1)实验1中用到的玻璃仪器主要有______________________________________(填名称)。
(2)由实验1可知,己烷的物理性质有____________________________________。
(3)实验2中的橙色溶液逐渐变浅的原因是__________________(填序号)。
A.己烷与溴发生了取代反应
B.溴代己烷为无色物质
C.液溴向外挥发浓度降低
D.己烷与液溴发生了加成反应
E.液溴与己烷分层,密度大的液溴在下层
(4)实验3中装置Ⅱ的作用是______________________________________。
(5)试管C中的现象是______________________________________。
(6)试写出装置Ⅰ中发生的生成丙烷和丙烯的化学方程式:______________________________________。
【答案】烧杯、分液漏斗(有无玻璃棒均正确) 己烷的密度比水小,难溶于水,可溶解溴 AB 冷凝己烷分解产生的气体 酸性高锰酸钾溶液的紫色褪去 ![]()
【解析】
(1)实验①的主要操作是分液,需要的玻璃仪器主要是烧杯和分液漏斗,故答案为:烧杯、分液漏斗;
(2)溴水和己烷混合后,下层几乎是无色的,且分液后得到橙色溶液,这说明己烷比水轻,难溶于水,可溶解溴,故答案为:己烷比水轻,难熔于水,可溶解溴;
(3)由于打开瓶盖瓶口出现白雾,这说明有溴化氢生成。由于己烷是烷烃,能和溴发生取代反应生成溴代烷和溴化氢,因此正确的答案选AB,故答案为:AB;
(4)实验3的装置Ⅱ中有冰水浴,所以该装置的作用是冷凝己烷分解产生的气体,故答案为:冷凝己烷分解产生的气体;
(5)己烷裂化有气态的烯烃生成,烯烃含有碳碳双键,能被酸性高锰酸钾溶液氧化,因此看到试管C中酸性高锰酸钾的紫色褪去,故答案为:酸性高锰酸钾的紫色褪去;
(6)在一定条件下,己烷裂化生成丙烷和丙烯,反应的化学方程式是CH3(CH2)4CH3 ![]() CH3CH2CH3﹢CH3CH=CH2,故答案为:CH3(CH2)4CH3
CH3CH2CH3﹢CH3CH=CH2,故答案为:CH3(CH2)4CH3 ![]() CH3CH2CH3﹢CH3CH=CH2。
CH3CH2CH3﹢CH3CH=CH2。

【题目】以下实验设计能达到实验目的的是( )
选项 | 实验目的 | 实验设计 |
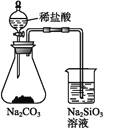
A | 证明非金属性强弱:Cl>C>Si |
|
B | 鉴别NaBr和KI溶液 | 分别加新制氯水后,用CCl4萃取 |
C | 除去NaHCO3固体中的Na2CO3 | 将固体加热至恒重 |
D | 证明相同温度下: Ksp(Ag2S)<Ksp(AgCl) | 向2 mL 0.1 mol·L-1硝酸银溶液中加入1 mL 0.1 mol·L-1 NaCl溶液,出现白色沉淀,再加入 几滴0.1 mol·L-1 Na2S溶液,有黑色沉淀生成 |
A.AB.BC.CD.D