题目内容
7.下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务.(1)甲、乙、丙三位同学分别设计了下列三套实验装置:
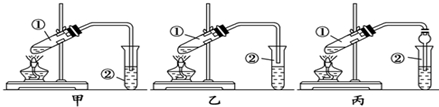
请从甲、乙两位同学设计的装置中选择一套作为实验室制取乙酸乙酯的装置,较合理的是乙(选填“甲”或“乙”),对比甲、乙装置,请分析丙装置的优点既能防止倒吸,又能充分吸收产物乙酸乙酯
(2)按所选择的装置组装仪器,在试管①中先加入3mL乙醇,并在振荡下缓缓加入2mL浓硫酸,冷却后再加入2mL冰醋酸,在试管②中加入适量的饱和Na2CO3溶液,对试管①加热.
?写出试管①中反应的化学方程式(注明反应条件)CH3COOH+CH3CH2OH
 CH3COOC2H5+H2O;
CH3COOC2H5+H2O;?试管②中饱和碳酸钠溶液的作用是B、C.
A.中和乙醇和乙酸 B.溶解乙醇并中和吸收乙酸
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中的小,有利于分层析出
D.加速酯的生成,提高其产率
?从试管②中分离出乙酸乙酯,应选择的装置是c.
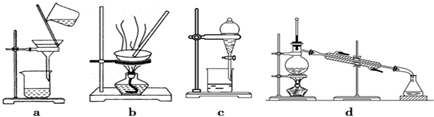
分析 (1)根据粗产品乙酸乙酯、乙酸和乙醇的混合物中各自的性质,以及加热不充分也能产生倒吸进行解答;
(2)酯化反应的本质为酸脱羟基,醇脱氢,乙醇、乙酸反应生成乙酸乙酯和水,且为可逆反应;用饱和碳酸钠溶液吸收乙酸乙酯,乙醇溶解,碳酸钠与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度;分离互不相溶的液体通常用分液的方法.
解答 解:(1)乙酸乙酯中混有乙醇和乙酸,二者易溶于水而产生倒吸,加热不充分也能产生倒吸,可用乙装置制取,防止倒吸回流现象的发生;丙同学将甲装置中的玻璃管改成了球形干燥管,除起冷凝充分吸收产物乙酸乙酯作用外,球形干燥管球形部分由于容积较大,也能起到防止倒吸的作用,
故答案为:乙;既能防止倒吸,又能充分吸收产物乙酸乙酯;
(2)酯化反应的本质为酸脱羟基,醇脱氢,乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应方程式为:CH3COOH+CH3CH2OH CH3COOC2H5+H2O,乙醇与乙酸都易挥发,制备的乙酸乙酯含有乙醇与乙酸,通常用饱和碳酸钠溶液吸收乙酸乙酯,中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,溶解挥发出来的乙醇,降低乙酸乙酯在水中的溶解度,便于分层得到酯,所以B、C正确,乙酸乙酯在上层,可用分液方法分离,需要用到的玻璃仪器主要是分液漏斗(可加烧杯),所以选择c装置,
CH3COOC2H5+H2O,乙醇与乙酸都易挥发,制备的乙酸乙酯含有乙醇与乙酸,通常用饱和碳酸钠溶液吸收乙酸乙酯,中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,溶解挥发出来的乙醇,降低乙酸乙酯在水中的溶解度,便于分层得到酯,所以B、C正确,乙酸乙酯在上层,可用分液方法分离,需要用到的玻璃仪器主要是分液漏斗(可加烧杯),所以选择c装置,
故答案为:CH3COOH+CH3CH2OH CH3COOC2H5+H2O;B、C;c.
CH3COOC2H5+H2O;B、C;c.
点评 本题考查乙酸乙酯的制备,题目难度中等,注意理解饱和碳酸钠溶液的作用以及酯化反应的机理,试题培养了学生分析、理解能力及灵活应用所学知识解决实际问题的能力.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
17.下表物质与其所含化学键类型、所属化合物类型完全正确的一组是( )
| 选 项 | A | B | C | D |
| 物 质 | MgCl2 | CO2 | HCl | NaOH |
| 所含化学键类型 | 离子键、共价键 | 共价键 | 离子键 | 离子键、共价键 |
| 所属化合物类型 | 离子化合物 | 共价化合物 | 离子化合物 | 共价化合物 |
| A. | A | B. | B | C. | C | D. | D |
18.下列装置对应实验的描述正确的是( )
| A | B | C | D |
 |  |  | 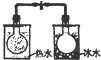 |
| 根据电流表(A)中指针是否偏转即可比较Zn,Cu的金属活泼性 | 根据小试管中液面的变化可判断铁钉发生了析氢腐蚀 | 根据温度计读数的变化测定浓硫酸和NaOH溶液反应的反应热 | 根据两烧瓶中气体颜色的变化(热水中变深、冰水中变浅)判断2NO2(g)?N2O4(g)是吸热反应 |
| A. | A | B. | B | C. | C | D. | D |
15.电解NO制备NH4NO3,其工作原理如图所示.下列说法不正确的是( )


| A. | 甲电极为阴极 | |
| B. | 为使电解产物全部转化为NH4NO3,需补充的物质为NH3 | |
| C. | 乙电极的电极反应式是:NO-3e-+4OH-=NO3-+2H2O | |
| D. | 该反应中NO既是氧化剂又是还原剂 |
2.“官能团”是决定有机物性质的原子或原子团,下列原子团不是“官能团”的是( )
| A. | -NH2 | B. | -CHO | C. | -COOH | D. | -CH2CH3 |
12.在同温同压下,下列各组热化学方程式中,△H2>△H1的是( )
| A. | 2H2(g)+O2(g)=2H2O(g)△H1; 2H2(g)+O2(g)=2H2O(l)△H2 | |
| B. | S(g)+O2(g)=SO2(g)△H1; S(s)+O2(g)=SO2(g)△H2 | |
| C. | $\frac{1}{2}$C(s)+O2(g)=CO(g)△H1; C(s)+O2(g)=CO2(g)△H2 | |
| D. | HCl(g)=$\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)△H1; H2(g)+Cl2(g)=2HCl(g)△H2 |