题目内容
2.下列反应对应的离子方程式正确的是( )| A. | 钠与水反应:Na+2H2O=Na++2OH-+H2↑ | |
| B. | 大理石与醋酸:CaCO3+2H+=Ca2++H2O+CO2 | |
| C. | 碳酸氢钙溶液中加入石灰水:Ca2++2HCO3-+2OH-=CaCO3+CO32-+2H2O | |
| D. | 明矾溶于水:Al3++3H2O?Al(OH)3+3H+ |
分析 A.离子方程式两边正电荷不相等,违反了电荷守恒;
B.醋酸为弱电解质,离子方程式中醋酸应该保留分子式;
C.钙离子足量,反应产物中不会有剩余的碳酸根离子;
D.明矾在溶液中电离出铝离子,铝离子水解生成的氢氧化铝胶体能够净水.
解答 解:A.钠与水反应生成氢氧化钠和氢气,正确的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,故A错误;
B.碳酸钙和醋酸都需要保留化学式,正确的离子方程式为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,故B错误;
C.碳酸氢钙溶液中加入石灰水,反应生成的碳酸根离子完全转化成碳酸钙沉淀,正确的离子方程式为:Ca2++HCO3-+OH-=CaCO3+H2O,故C错误;
D.明矾的净水原理为:Al3++3H2O?Al(OH)3+3H+,故D正确;
故选D.
点评 本题考查了离子方程式的书写判断,为中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
相关题目
12.下列各组稀溶液:①氨水和硝酸银 ②NaAlO2和盐酸 ③硫酸氢钠和氢氧化钡 ④硝酸和碳酸钠.只用试管、滴管及闻气味就能鉴别的是( )
| A. | ③④ | B. | ①②④ | C. | ①②③④ | D. | ②④ |
13.下列各组气体,通常情况下能共存,并且能用浓硫酸和碱石灰干燥的是( )
| A. | H2、O2 | B. | SO2、H2S | C. | NO、O2 | D. | HCl、NH3 |
10.短周期元素A、B、C、D的原子序数依次递增,它们的核电荷数之和为32,原子最外层电子数之和为10.A与C同主族,B与D同主族,A、C原子的最外层电子数之和等于B原子的次外层电子数.则下列叙述正确的是( )
| A. | 四种元素的原子半径:A<B<D<C | |
| B. | D元素处于元素周期表中第3周期第ⅥA族 | |
| C. | B、D的最高价氧化物中,B、D与氧原子之间均为双键 | |
| D. | 一定条件下,D单质能置换出B单质,C单质能置换出A单质 |
17.将SO2气体通入下列物质中,不可能发生氧化还原反应的是( )
| A. | FeCl3 | B. | H2O2溶液 | C. | 浓H2SO4 | D. | Na2S溶液 |
7.用胶头滴管向用石蜡围成的“spark”凹槽内注入某溶液,即可在玻璃上刻蚀出“spark”的字样,则该溶液是( )
| A. | 盐酸 | B. | 氢氟酸 | C. | 烧碱 | D. | 饱和食盐水 |
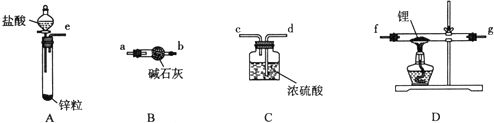
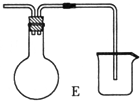
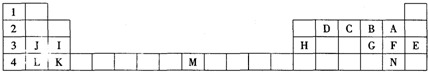
 .
.