题目内容
8.盐酸、硫酸和硝酸都是重要的化工原料,也是化学实验室里必备的重要试剂.请回答下列问题:(1)常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有强氧化性.用玻璃棒蘸取浓硫酸滴在纸上,纸逐渐变黑,说明浓硫酸具有脱水性.
(2)硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,工业上用洗净的废铜屑作原料来制备硝酸铜.下列制备方法符合“绿色化学”思想的是③(填序号).
①Cu+HNO3(浓)→Cu(NO3)2
②Cu+HNO3(稀)→Cu(NO3)2
③Cu$→_{△}^{空气}$CuO$\stackrel{HNO_{3}(稀)}{→}$Cu(NO3)2
(3)①在100mL 18mol•L-1的浓硫酸中加入过量的铜片,加热使之充分反应,测得产生的气体在标准状况下的体积可能是D.
A.40.32L B.30.24L C.20.16L D.13.44L
②若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O.
(4)若将12.8g铜跟一定质量的浓HNO3反应,铜消耗完时,共产生气体5.6L(标准状况),则所耗HNO3的物质的量0.65mol
(5)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水.该反应的化学方程式为Cu+2HCl+H2O2=CuCl2+2H2O.
分析 (1)浓硫酸具有强氧化性和脱水性,根据其特性来回答判断;
(2)“绿色化学”思想指的是化学反应中没有污染性的物质生成、原子利用率高的反应;
(3)浓硫酸中加入过量的铜片,随着反应的进行,浓硫酸浓度减小,金属铜和稀硫酸不反应,在硫酸存在时,再加入硝酸钠,相当于存在了硝酸;
(4)铜和硝酸反应生成硝酸铜与氮的氧化物(NO或NO2或NO、NO2的混合物),反应中硝酸其氧化剂、酸性作用,起氧化剂作用的硝酸生成氮的氧化物,起酸性作用的硝酸生成Cu(NO3)2,根据氮原子守恒:2n[Cu(NO3)2]+n(NO、NO2),据此计算消耗硝酸的物质的量;
(5)双氧水具有氧化性,在酸性环境下可以将金属铜氧化;
解答 解:(1)常温下,可用铁、铝制的容器盛放浓硫酸,浓硫酸具有强氧化性,而使得金属表明形成一层致密的氧化膜,阻止反应的发生,用玻璃棒蘸取浓硫酸滴在纸上,纸逐渐变黑,是浓硫酸脱水性的表现,故答案为:强氧化;脱水;
(2)“绿色化学”思想指的是化学反应中没有污染性的物质生成、原子利用率高的反应,在反应①②中会有污染性的气体一氧化氮和二氧化氮生成,只有制备方法③符合“绿色化学”思想,故答案为:③;
(3)①浓硫酸中加入过量的铜片,发生反应Cu+2H2SO4=CuSO4+SO2↑+2H2O,100mL 18mol•L-1的浓硫酸理论上完全反应,会产生二氧化硫0.9mol,体积为:0.9mol×22.4L/mol=20.16L,但是随着反应的进行,浓硫酸浓度减小,金属铜和稀硫酸不反应,所以试剂测得产生的气体在标准状况下的体积会小于20.16L,只有D正确,故答案为:D;
②在硫酸存在时,再加入硝酸钠,相当于存在了硝酸,金属铜可以和硝酸发生反应生成硝酸铜和一氧化氮,反应实质是:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,
故答案为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
(4)12.8gCu的物质的量=$\frac{12.8g}{64g/mol}$=0.2mol,气体的物质的量=$\frac{5.6L}{22.4L/mol}$=0.25mol,
根据氮原子守恒,n(HNO3)=2n[Cu(NO3)2]+n(NO、NO2)=2×0.2mol+0.25mol=0.65mol;
故答案为:0.65;
(5)双氧水具有氧化性,在酸性环境下可以将金属铜氧化,发生反应的原理方程式是:Cu+2HCl+H2O2=CuCl2+2H2O,故答案为:Cu+2HCl+H2O2=CuCl2+2H2O.
点评 本题考查了浓硫酸、浓硝酸的性质,以及有关硝酸的计算,难度中等,注意利用氮原子个数守恒是解题关键.


| A. | 含1mol HPE的溶液最多可以和2molNaOH反应 | |
| B. | HPE不能跟浓溴水反应 | |
| C. | 1molHPE能与4molH2发生加成反应 | |
| D. | HPE分子中最多有12个原子共平面 |
| A. | 1:9 | B. | 1:49 | C. | 1:99 | D. | 以上都不正确 |
| A. | 用惰性电极电解饱和氯化钠溶液:2Cl-+2H+ $\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑ | |
| B. | 用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | 利用腐蚀法制作印刷线路板:2Fe3++Cu═2Fe2++Cu2+ | |
| D. | 实验室用液溴和苯在催化剂作用下制溴苯: |
| A. | 使用的NaOH固体在空气中敞口放置了一段时间 | |
| B. | 容量瓶用蒸馏水洗净后,未经干燥 | |
| C. | 在烧杯中溶解NaOH后,未经冷却即将溶液转入容量瓶 | |
| D. | 调节天平零点时未将游码回到最左边 |
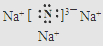 .
.


 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$
 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +2H2O.
+2H2O.