题目内容
20.下列文字表述与反应方程式对应且正确的是( )| A. | 用惰性电极电解饱和氯化钠溶液:2Cl-+2H+ $\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑ | |
| B. | 用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | 利用腐蚀法制作印刷线路板:2Fe3++Cu═2Fe2++Cu2+ | |
| D. | 实验室用液溴和苯在催化剂作用下制溴苯: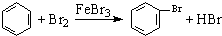 |
分析 A.电解饱和食盐水生成氯气和氢气,氢氧化钠,离子方程式水不能拆开;
B.醋酸为弱酸,应写成化学式;
C.根据离子方程式原子守恒、电荷也守恒判断;
D.液溴与苯在催化剂条件下发生取代反应生成溴苯和HBr.
解答 解:A.电解饱和食盐水生成氯气和氢气,氢氧化钠,反应式为2Cl-+2H2O $\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2OH-,离子方程式水不能拆开,故A错误;
B.醋酸为弱酸,应写成化学式,正确的离子方程式为CaCO3+2CH3COOH=2CH3COO-+Ca2++H2O+CO2↑,故B错误;
C.该离子方程式原子守恒、电荷也守恒,故C正确;
D.液溴与苯在催化剂条件下发生取代反应生成溴苯和HBr,反应的方程式为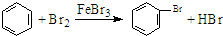 ,故D正确.
,故D正确.
故选CD.
点评 本题考查离子方程式以及化学方程式的书写,题目难度不大,本题注意离子的检验方法,离子方程式中的弱电解质、电荷守恒等问题.

练习册系列答案
相关题目
10.设NA为阿伏加德罗常数的数值,下列说法错误的是( )
| A. | NA 个氨气分子中含有3mol σ 键 | |
| B. | 18g水中含有NA 对孤电子对 | |
| C. | NA 个氮气分子中含有2mol π键 | |
| D. | NA 个二氧化碳分子中含有2mol π键 |
15. 四种短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y是地球上含量最高的金属元素.下列判断正确的是( )
四种短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y是地球上含量最高的金属元素.下列判断正确的是( )
 四种短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y是地球上含量最高的金属元素.下列判断正确的是( )
四种短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y是地球上含量最高的金属元素.下列判断正确的是( )| A. | 1molW的单质在足量空气中燃烧转移电子数是6NA | |
| B. | 含Y元素的盐溶液可能显酸性,也可能显碱性 | |
| C. | Z元素的单质和氧化物不能与任何酸发生反应 | |
| D. | X与H、O元素形成的化合物一定是共价化合物 |
5.Ⅰ.2011年11月28日至12月9日,联合国气候变化框架公约第17次缔约方会议在南非德班召开,随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.
(1)目前工业上有一种方法是用CO2来生产燃料甲醇.为探究该反应原理,进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3.25mol H2,在一定条件下发生反应,测定CO2、CH3OH(g)和H2O (g)的浓度随时间变化如图所示:
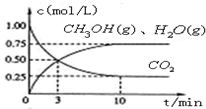
①写出该工业方法制取甲醇的化学反应方程式CO2+3H2?CH3OH+H2O.
②从反应开始到平衡,氢气的平均反应速率v (H2)=0.225mol•L-1•min-1.当温度降低时CO2的转化率变大,则该反应△H<0(填“>”“<”或“=”).
③下列措施中能使n(CH3OH)/n(CO2)增大的是C.
A.升高温度 B.充入氮气 C.将水蒸气从体系中分离 D.用更有效的催化剂
(2)选用合适的合金作为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此燃料电池负极的电极方程式为CH3OH-6 e-+8OH-=CO32-+6H2O.
Ⅱ:已知下列物质在20℃下的Ksp如下,试回答下列问题:
(1)20℃时,上述五种银盐饱和溶液中,Ag+物质的量浓度由大到小的顺序是Ag2CrO4>AgCl>AgBr>AgI>Ag2S.
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,$\frac{c(Βρ-)}{c(Χλ-)}$=2.7×10-3.
(3)测定水体中氯化物含量,常用标准硝酸银法进行滴定,滴定时应加入的指示剂_D.
A.KBr B.KI C.K2S D.K2CrO4.
(1)目前工业上有一种方法是用CO2来生产燃料甲醇.为探究该反应原理,进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3.25mol H2,在一定条件下发生反应,测定CO2、CH3OH(g)和H2O (g)的浓度随时间变化如图所示:

①写出该工业方法制取甲醇的化学反应方程式CO2+3H2?CH3OH+H2O.
②从反应开始到平衡,氢气的平均反应速率v (H2)=0.225mol•L-1•min-1.当温度降低时CO2的转化率变大,则该反应△H<0(填“>”“<”或“=”).
③下列措施中能使n(CH3OH)/n(CO2)增大的是C.
A.升高温度 B.充入氮气 C.将水蒸气从体系中分离 D.用更有效的催化剂
(2)选用合适的合金作为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此燃料电池负极的电极方程式为CH3OH-6 e-+8OH-=CO32-+6H2O.
Ⅱ:已知下列物质在20℃下的Ksp如下,试回答下列问题:
| 化学式 | 颜色 | Ksp |
| AgCl | 白色 | 2.0×10-10 |
| AgBr | 浅黄色 | 5.4×10-13 |
| AgI | 黄色 | 8.3×10-17 |
| Ag2S | 黑色 | 2.0×10-48 |
| Ag2CrO4 | 红色 | 2.0×10-12 |
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,$\frac{c(Βρ-)}{c(Χλ-)}$=2.7×10-3.
(3)测定水体中氯化物含量,常用标准硝酸银法进行滴定,滴定时应加入的指示剂_D.
A.KBr B.KI C.K2S D.K2CrO4.
12.表示下列变化的化学用语正确的是( )
| A. | 乙烯的分子式:CH2=CH2 | |
| B. | NaHCO3的电离:HCO3-+H2O?H3O++CO32- | |
| C. | NaOH的结构式:Na-O-H | |
| D. | NH4Cl的电子式: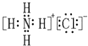 |
12.下表为元素周期表中的一部分,用化学式或元素符号回答下列问题:
(1)10种元素中,化学性质最不活泼的是Ar;
(2)④②⑤中,最高价氧化物的水化物,碱性最强的碱是KOH;
(3)②④⑦中形成的简单离子,半径由大到小的顺序是S2->K+>Ca2+;
(4)写出①与⑦形成的最简单化合物的电子式 .
.
(5)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为NaOH+Al(OH)3=Na[Al(OH)4]
(6)试比较与⑦与⑧两种元素最简单氢化物的沸点高低H2O>H2S.
(7)设计一个简单实验证明⑦⑨两种元素非金属性强弱的比较把溴水加到Na2S(或氢硫酸)溶液中,出现淡黄色沉淀;从而证明Br的非金属性强于S的.
| 族 周期 | I A | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑧ | ||||||
| 3 | ① | ③ | ⑤ | ⑦ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)④②⑤中,最高价氧化物的水化物,碱性最强的碱是KOH;
(3)②④⑦中形成的简单离子,半径由大到小的顺序是S2->K+>Ca2+;
(4)写出①与⑦形成的最简单化合物的电子式
 .
.(5)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为NaOH+Al(OH)3=Na[Al(OH)4]
(6)试比较与⑦与⑧两种元素最简单氢化物的沸点高低H2O>H2S.
(7)设计一个简单实验证明⑦⑨两种元素非金属性强弱的比较把溴水加到Na2S(或氢硫酸)溶液中,出现淡黄色沉淀;从而证明Br的非金属性强于S的.
