题目内容
(1)(4分)写出下列物质在水溶液中的电离方程式:
HNO3 Ba(OH)2
NaHCO3 NaHSO4
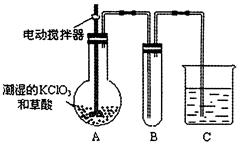
(2)(4分)在实验室制备氯气的过程中,多余的氯气通常是用氢氧化钠溶液进行吸收,请写出此反应的化学方程式并标出电子转移的方向和数目。
该化学反应中,氧化剂是 ,还原剂是 。
(1)(4分) HNO3=H++NO3– Ba(OH)2=Ba2++2OH–
NaHCO3=Na++HCO3– NaHSO4=Na++H++SO42–
(2)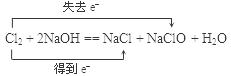 Cl2 Cl2
Cl2 Cl2
解析试题分析:(1)酸能电离出H+和酸根离子,故HNO3电离方程式为:HNO3=H++NO3–;碱电离出金属离子和OH–,故Ba(OH)2电离方程式为:Ba(OH)2=Ba2++2OH–;弱酸的酸式盐电离时产生的是金属离子和酸式酸根离子,故NaHCO3电离方程式为:NaHCO3=Na++HCO3–;强酸的酸式盐能完全电离出H+,故NaHSO4电离方程式为:NaHSO4=Na++H++SO42–。
(2)在氯气跟氢氧化钠溶液的反应中,氯元素的化合价既降低(由0价降到–1价)又升高(由0价升到+1价),所以氯气既是氧化剂又是还原剂。
考点:考查电离方程式的书写、氧化还原反应的表示方法及氧化剂和还原剂的判断。

 阅读快车系列答案
阅读快车系列答案有一无色透明的溶液,要确定是否含有以下离子:K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,取该溶液实验如下:
| 实验步骤 | 实验现象 |
| (1)取少量该溶液,加几滴甲基橙 | 溶液变红色 |
| (2)取少量该溶液加热浓缩,加Cu片和浓H2SO4,加热 | 有无色气体产生,气体遇空气可以变成红棕色 |
| (3)取少量该溶液,加BaCl2溶液 | 有白色沉淀生成 |
| (4)取(3)中上层清液,加AgNO3溶液 | 有稳定的白色沉淀生成,且不溶于HNO3 |
| (5)取少量该溶液,加NaOH溶液 | 有白色沉淀生成,当NaOH过量时沉淀部分溶解 |
由此判断:
(1)溶液中肯定存在的离子是___________________________________________________________,溶液中肯定不存在的离子是__________________________________________________________________。
(2)为进一步确定其他离子,应该补充的实验及对应欲检离子的名称(如为溶液反应,说明使用试剂的名称,不必写详细操作步骤)。_________________________________________________________。
1L某混合溶液,可能含有的离子如下表:
| 可能大量含有的阳离子 | H+、Ag+、Mg2+、Al3+、NH4+、Fe3+ |
| 可能大量含有的阴离子 | Cl-、Br-、I-、CO32-、Al(OH)4-(或AlO2-) |
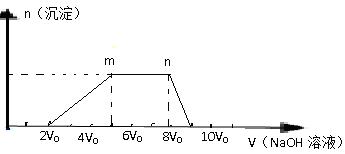
(1)该溶液中一定不存在的阳离子是 。
(2)该溶液中一定不存在的阴离子是 。
(3)m→n反应的的离子方程式为 。
(4)溶液中含有的阳离子对应的物质的量比为 。
Ⅱ、经检测,该溶液中还含有大量的Cl-、Br-、I-,向混合溶液中加入足量的氯化铁溶液,请写出有关反应的离子方程式 。
 ,可选用Ba(OH)2、HCl和K2CO3三种试剂,按如下步骤操作:
,可选用Ba(OH)2、HCl和K2CO3三种试剂,按如下步骤操作: 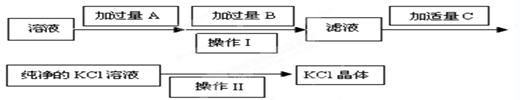
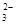 、OH-、HCO
、OH-、HCO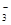 、Cl-等离子中的若干种。为了确定溶液的组成,进行了如下操作:
、Cl-等离子中的若干种。为了确定溶液的组成,进行了如下操作: