��Ŀ����
���ձ���ʢ�а뱭��Ba��OH��2��Һ��Ȼ���õι����ձ��еμ�H2SO4��װ������ͼ������������ĵ��룬��ƻ��䰵��������ǡ����ȫ��Ӧʱ�������ȫϨ��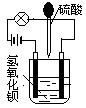
��1����ʵ��˵����Һ�ĵ�������_________________�йء�
��2��������Ӧ�����ӷ���ʽΪ_________________________________________��
��3��������������ԭ��������ҺŨ�ȵIJⶨ�����ձ���װ��75mL 0��1mol/L Ba��OH��2��Һ��������25mL H2SO4ʱ�������ȫϨ�������������Һ�����ʵ���Ũ�ȡ�
��4������98%��1��84g/mL��Ũ������������Ũ�ȵ�������Һ2500mL����Ҫ���ٺ�����Ũ���ᣨ��ȷ��0��1mL)��
��1������Ũ�ȣ�2�֣�
��2��Ba2++2OH-+2H++SO42-=BaSO4��+2H2O��3�֣�
��3��0��3mol/L��5�֣�
��4��40��8mL��4�֣�
���������������ϡ������Һ�������μ�����������Һֱ�����������ڷ����˷�Ӧ��Ba(OH)2 +H2SO4�TBaSO4��+2H2O����������������Һ�ĵμӣ�����Ũ����С�����������ͣ��������Ϊ�㣬Ҳ����˵ǡ����ȫ��Ӧʱû�������ƶ��������ˣ��������ʹ��������ܹ������ˣ���Һ����Һ�ĵ����Ա仯��ǿ������ˮ�����ĵ����ԣ���ǿ��
�Ÿ�ʵ��˵����Һ�ĵ�����������Ũ���йأ��𰸣�����Ũ�ȣ���������Ӧ�����ӷ���ʽΪ��Ba2++2OH-+2H++SO42-==BaSO4��+2H2O���𰸣�Ba2++2OH-+2H++SO42-==BaSO4��+2H2O���ǵ����ȫϨ��˵����Ӧ�պ���ȫ���У��ɷ���ʽ��֪��
Ba(OH)2 + H2SO4�TBaSO4��+2H2O
1 1
75mL��0��1mol/L C��25mL
75mL��0��1mol/L=C��25mL
C=0��3mol/L
�𰸣�0��3mol/L��
������98%��1��84g/L��Ũ������������Ũ�ȵ�������Һ2500mL��ŨH2SO4�����ʵ���Ũ��c=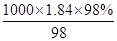 mol��L��1=18��4mol��L��1������ϡ�Ͷ��ɣ�ϡ��ǰ�����ʵ����ʵ������䣬������Ũ������������Ũ��������ΪxmL������xmL��18��4mol��L��1=2500mL��0��3mol��L��1����ã�x��40��8������Ӧ��ȡ��Ũ���������40��8mL���𰸣�40��8mL��
mol��L��1=18��4mol��L��1������ϡ�Ͷ��ɣ�ϡ��ǰ�����ʵ����ʵ������䣬������Ũ������������Ũ��������ΪxmL������xmL��18��4mol��L��1=2500mL��0��3mol��L��1����ã�x��40��8������Ӧ��ȡ��Ũ���������40��8mL���𰸣�40��8mL��
���㣺�������Һ�ĵ����ԣ�ϡ�Ͷ���

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д���֪����������Һ�пɷ��������������ӷ�Ӧ��Ge4����Fe2��===Fe3����Ge3���� Sn2����2Fe3��===2Fe2����Sn4�����ɴ˿���ȷ��Fe2����Ge3����Sn2���������ӵĻ�ԭ����ǿ������˳����
| A��Sn2����Fe2����Ge3�� | B��Sn2����Ge3����Fe2�� |
| C��Ge3����Fe2����Sn2�� | D��Fe2����Sn2����Ge3�� |
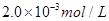 �������������Һ10.0mL��ǡ����ȫ��Ӧ���жϷ�Ӧ��ȫ��ʵ������Ϊ____________________________________,��üӵ�����Ʒ�е�Ԫ�صĺ���Ϊ______________________mg/Kg(�ú�w�Ĵ���ʽ��ʾ)��
�������������Һ10.0mL��ǡ����ȫ��Ӧ���жϷ�Ӧ��ȫ��ʵ������Ϊ____________________________________,��üӵ�����Ʒ�е�Ԫ�صĺ���Ϊ______________________mg/Kg(�ú�w�Ĵ���ʽ��ʾ)��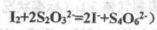 ��
��
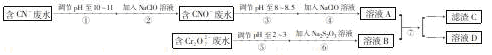
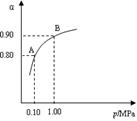
 2SO3(g)����H��0��550 ��ʱ��SO2ת��ΪSO3��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ��ʾ��
2SO3(g)����H��0��550 ��ʱ��SO2ת��ΪSO3��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ��ʾ��