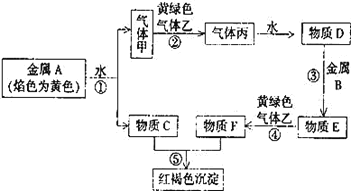
题目内容
【题目】某课外活动小组在实验室用如下图所示的装置进行实验,验证氨的某些性质并收集少量纯净的N2。
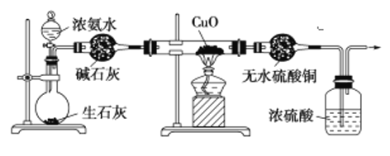
请回答:
(1)实验前先将仪器按图示连接好,然后检查装置的气密性。怎样检查该装置的气密性?________________。
(2)烧瓶内装有生石灰,随浓氨水的滴入,产生氨气。氨气产生的原因是________________。
(3)实验进行一段时间后,观察到加热的硬质玻璃管内的黑色氧化铜粉末变为红色,盛无水CuSO4的干燥管内出现蓝色,并且在最后的出气导管处收集到纯净、干燥的N2。根据这些现象,写出硬质玻璃管内发生反应的化学方程式:______________________。这个反应说明氨气具有________。
A.碱性 B.还原性 C.氧化性 D.不稳定性
(4)洗气瓶中浓硫酸的主要作用是________________________。
(5)在最后出气管的导管口收集干燥、纯净的氮气,收集方法是___________________。
【答案】先关闭分液漏斗的活塞,向广口瓶中加水,浸没进气导管口,用酒精灯在烧瓶下稍加热,若导气管口有少量气泡冒出,停止加热后,导管内水面上升,形成一段水柱,说明装置的气密性良好 NH3·H2O中的H2O与CaO反应并放热,使NH3逸出 3CuO+2NH3![]() 3Cu+N2+3H2O B 干燥N2,吸收未反应的NH3 用塑料袋或球胆收集
3Cu+N2+3H2O B 干燥N2,吸收未反应的NH3 用塑料袋或球胆收集
【解析】
浓氨水和生石灰可以快速制氨气之后碱石灰干燥氨气,直型玻璃管中发生氨气还原氧化铜的反应,黑色粉末变红说明生成了铜,无水硫酸铜变蓝说明生成了水,同时还有氮气生成。
(1)检查本装置气密性,先关闭分液漏斗的活塞,向广口瓶中加水,浸没进气导管口,用酒精灯在烧瓶下稍加热,若导气管口有少量气泡冒出,停止加热后,导管内水面上升,形成一段水柱,说明装置的气密性良好,故答案为:先关闭分液漏斗的活塞,向广口瓶中加水,浸没进气导管口,用酒精灯在烧瓶下稍加热,若导气管口有少量气泡冒出,停止加热后,导管内水面上升,形成一段水柱,说明装置的气密性良好;
(2)浓氨水滴入生石灰中,生石灰CaO溶于水放热,使氨水分解同时生石灰与水反应生成氢氧化钙,氢氧根离子浓度增大,使NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH4++OH-电离平衡向左移动,氨气逸出,所以用浓氨水和生石灰可以快速制氨气,故答案为:NH3·H2O中的H2O与CaO反应并放热,使NH3逸出;
NH4++OH-电离平衡向左移动,氨气逸出,所以用浓氨水和生石灰可以快速制氨气,故答案为:NH3·H2O中的H2O与CaO反应并放热,使NH3逸出;
(3)碱石灰的作用是干燥氨气,E中发生氨气还原氧化铜的反应,黑色粉末变红说明生成了铜,无水硫酸铜变蓝说明生成了水,同时还有氮气生成,由此可写出反应方程式3CuO+2NH3![]() 3Cu+N2+3H2O,反应中-3价的氮全部升为0价,氨气表现还原性,故答案为:3CuO+2NH3
3Cu+N2+3H2O,反应中-3价的氮全部升为0价,氨气表现还原性,故答案为:3CuO+2NH3![]() 3Cu+N2+3H2O;B;
3Cu+N2+3H2O;B;
(4)洗气瓶中浓硫酸的作用是干燥N2、吸收多余的氨气,防止氨气逸出污染环境,故答案为:干燥N2;吸收未反应的NH3;
(5)收集纯净、干燥的氨气用气囊收集,故可用塑料袋或球胆收集,故答案为:用塑料袋或球胆收集。