题目内容
【题目】现有下列3种有机物:
① CH2=CH2 ② CH3CH2Br ③ ![]()
(1)其中具有弱酸性的是____(填序号),与Na2CO3溶液反应的化学方程式是_________。
(2)能发生消去反应的是____(填序号),反应方程式是____________。
(3)能发生加聚反应的是____(填序号),反应方程式是_______。
【答案】③ ![]() + Na2CO3→ NaHCO3+
+ Na2CO3→ NaHCO3+![]() ② CH3CH2Br + NaOH
② CH3CH2Br + NaOH ![]() CH2=CH2↑+NaBr+H2O ① n CH2=CH2
CH2=CH2↑+NaBr+H2O ① n CH2=CH2 ![]()
![]()
【解析】
(1)含-COOH、酚-OH的有机物具有酸性;
(2)-OH、-X相连C的邻位C上有H可发生消去反应;
(3)上述物质中含双键的有机物可发生加聚反应。
(1)其中具有弱酸性的是③,与Na2CO3溶液反应的化学方程式是![]() + Na2CO3→ NaHCO3+
+ Na2CO3→ NaHCO3+![]() ;
;
(2)能发生消去反应的是②,反应方程式是CH3CH2Br+NaOH![]() CH2=CH2↑+NaBr+H2O;
CH2=CH2↑+NaBr+H2O;
(3)能发生加聚反应的是①,反应方程式是![]() 。
。

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案【题目】七水硫酸镁(MgSO4·7H2O)在印染、造纸和医药等工业上有重要的用途。硼镁泥是硼镁矿生产硼砂的废渣,其主要成分是MgCO3,还含有MgO、CaO、Fe2O3、FeO、MnO2、Al2O3、SiO2等杂质,工业上用硼镁泥制取七水硫酸镁的工艺流程如图:
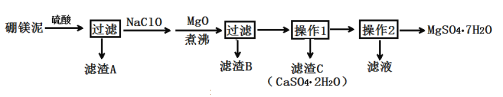
已知:①MnO2不溶于稀硫酸。
②CaSO4和MgSO4·7H2O在不同温度下的溶解度(g)数据如下表所示:
温度/℃ 物质 | 10 | 30 | 40 | 50 | 60 |
CaSO4 | 0.19 | 0.21 | 0.21 | 0.21 | 0.19 |
MgSO4·7H2O | 30.9 | 35.5 | 40.8 | 45.6 | —— |
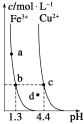
(1)开始用到硫酸的质量分数为70%,密度为1.61g/cm3,则该硫酸溶液的物质的量浓度为___。
(2)滤渣A中除含少量CaSO4·2H2O外,还有___。
(3)加入MgO后,加热煮沸的目的是___。
(4)若滤渣B的主要成分为Al(OH)3和Fe(OH)3。则加入NaClO发生氧化还原反应的离子方程式为___。
(5)流程中操作1为蒸发浓缩、趁热过滤,这样即可得到CaSO4·2H2O,又防止___。
(6)获取MgSO4·7H2O的操作2为:___、___、过滤洗涤。
(7)已知开始硼镁泥样品的质量为ag,制取七水硫酸镁的质量为bg,据此能计算出硼镁泥中镁元素的含量吗?若能,请写出表达式;若不能,请说明理由。___(能或不能),表达式(或理由)为___。