题目内容
【题目】某温度时在2L容器中X、Y、Z三种物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据
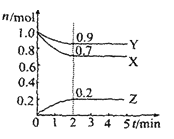
(1)该反应的化学方程式为:_____
(2)反应开始至2min,用Z表示的平均反应速率为:____
(3)下列叙述能说明上述反应达到化学平衡状态的是____(填序号)
A.混合气体的总物质的量不随时间的变化而变化
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗3mol X,同时生成2mol Z
D.混合气体的总质量不随时间的变化而变化
(4)在密闭容器里,通入a mol X(g)和b mol Y(g),发生反应X(g) + Y(g) = 2Z(g),当改变下列条件时,反应速率会发生什么变化(选填“增大”、“减小”或“不变”)?
①降低温度:____
②加入催化剂:____
③增大容器的体积:____
【答案】3X + Y![]() 2Z 0.05 mol·L-1·min-1 AB 减小 增大 减小
2Z 0.05 mol·L-1·min-1 AB 减小 增大 减小
【解析】
利用坐标图象推断X、Y、Z发生反应的化学方程式时,首先从图象的起点切入,依据物质的量的变化趋势确定反应物和生成物,其次利用各物质的物质的量的变化量,确定化学计量数,最后依据反应结束后是否存在某一物质的量为0,确定反应是可逆反应还是不可逆反应。利用某量判断平衡状态时,需分析题中所给的量是常量还是变量,变量不变是平衡状态;分析条件改变对反应速率的影响时,需分析条件改变后,能否引起分子碰撞次数的增大或活化能的降低。
(1)从反应起点看,X 、 Y为反应物,Z为生成物;从变化量之比等于化学计量数之比分析,化学计量数为3X+ Y→2Z;从反应的最终结果看,没有一种物质的物质的量为0,所以反应可逆,因此该反应的化学方程式为:3X + Y![]() 2Z。答案为:3X + Y
2Z。答案为:3X + Y![]() 2Z;
2Z;
(2)反应开始至2min,用Z表示的平均反应速率为: =0.05 mol·L-1·min-1。答案为:0.05 mol·L-1·min-1;
=0.05 mol·L-1·min-1。答案为:0.05 mol·L-1·min-1;
(3)A.随着反应的进行,混合气体的总物质的量减小,当物质的量不变时,反应达平衡状态,A符合题意;
B.随着反应的进行,气体的总物质的量不断减小,混合气体的压强不断减小,当混合气体的压强不变时,气体的物质的量不变,反应达平衡状态,B符合题意;
C.不管反应是否达平衡,单位时间内每消耗3mol X,同时生成2mol Z,此时反应不一定达平衡状态,C不合题意;
D.不管反应进行到什么程度,混合气体的总质量都保持不变,所以混合气体总质量不变时,不一定达平衡状态,D不合题意;
故选AB。答案为:AB;
(4) ①降低温度:反应物的能量降低,有效碰撞次数减少,反应速率减小;
②加入催化剂:降低反应的活化能,增大活化分子百分数,化学反应速率加快;
③增大容器的体积:减小反应混合物的浓度,分子有效碰撞的次数减少,反应速率减慢;
答案为:减小;增大;减小。

【题目】七水硫酸镁(MgSO4·7H2O)在印染、造纸和医药等工业上有重要的用途。硼镁泥是硼镁矿生产硼砂的废渣,其主要成分是MgCO3,还含有MgO、CaO、Fe2O3、FeO、MnO2、Al2O3、SiO2等杂质,工业上用硼镁泥制取七水硫酸镁的工艺流程如图:
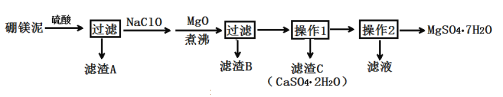
已知:①MnO2不溶于稀硫酸。
②CaSO4和MgSO4·7H2O在不同温度下的溶解度(g)数据如下表所示:
温度/℃ 物质 | 10 | 30 | 40 | 50 | 60 |
CaSO4 | 0.19 | 0.21 | 0.21 | 0.21 | 0.19 |
MgSO4·7H2O | 30.9 | 35.5 | 40.8 | 45.6 | —— |
(1)开始用到硫酸的质量分数为70%,密度为1.61g/cm3,则该硫酸溶液的物质的量浓度为___。
(2)滤渣A中除含少量CaSO4·2H2O外,还有___。
(3)加入MgO后,加热煮沸的目的是___。
(4)若滤渣B的主要成分为Al(OH)3和Fe(OH)3。则加入NaClO发生氧化还原反应的离子方程式为___。
(5)流程中操作1为蒸发浓缩、趁热过滤,这样即可得到CaSO4·2H2O,又防止___。
(6)获取MgSO4·7H2O的操作2为:___、___、过滤洗涤。
(7)已知开始硼镁泥样品的质量为ag,制取七水硫酸镁的质量为bg,据此能计算出硼镁泥中镁元素的含量吗?若能,请写出表达式;若不能,请说明理由。___(能或不能),表达式(或理由)为___。