��Ŀ����
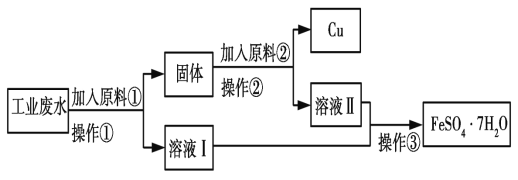
����Ŀ��ij�о�С��ͬѧΪ̽��п�����ᷴӦ����SO2��H2���ٽ�Ũ��(Ũ��������п��Ӧ����SO2�����Ũ��)���������ʵ�顣�ڴ��Թ�A�м���100mLl 8mol/L���ᣬ�����������ϰ��ϵĶ���������ڼ���������п��(���ϰ����������ƶ�)�����Լ�ƿD�м���������ŨNaOH��Һ(���Ⱥͼг�װ����ʡ��)��

��֪��п��Ũ����Ӵ�����ʼʱ��Ӧ�����������ʵ������Լ����䷴Ӧ�����д�����������ʱ���÷�Ӧ���ʻ����Լӿ첢���д������ȷų���
(1)��д��п�����ᷴӦ����SO2�Ļ�ѧ����ʽ______________��
(2)����װ����֮�����Լ�֮ǰ������еIJ�����__________��
(3)������B��������______�����û�������ƣ����ղⶨ���ٽ�Ũ�Ȼ�_________��(����ƫ��������ƫ��"������Ӱ����)
(4)װ���и����C��������_______�����������ж������Ѵ��ٽ�Ũ��________��
(5)��Ӧ��������Dװ���м���������H2O2��Һ��������BaCl2��Һ����ַ�Ӧ�����ó������ˡ�ϴ�ӡ���������õ���������Ϊa�ˣ���Ũ������п��Ӧ���ٽ�Ũ��Ϊ��_________mol/L��(�ú�a�ļ���ʽ��ʾ����������仯)
(6)ijͬѧͨ����ϵ������ԭ��Ӧ�����֪ʶ����ΪҲ�������������ữ�ĸ��������Һ��D�е�SO32-���еζ���ͨ���ζ�����SO32-�����ʵ��������ٽ�Ũ�ȣ�����Ϊ������һ�뷨�Ƿ����?________(����������������������)��ԭ����__________��
���𰸡�Zn+2H2SO4(Ũ)=ZnSO4+SO2��+2H2O ����װ�������� �������������� ƫ�� ������ ��F���ռ����岢�鴿�����ȷ���ռ�����������֤������Ũ���Ѿ������ٽ������ 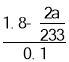 ������ ʵ������в��ܱ�֤�õ���Na2SO3��Һ�Ƿ�ᱻ�����е������������ʣ���ɵζ������ȷ
������ ʵ������в��ܱ�֤�õ���Na2SO3��Һ�Ƿ�ᱻ�����е������������ʣ���ɵζ������ȷ
��������
���ʵ��̽��п�����ᷴӦ����SO2��H2���ٽ�Ũ�ȣ���Ϊ��װ����һ�����巢��װ�ã�����װ����֮����װ������֮����װ�������ԣ�����������п��Ӧ���ɶ�����������Ũ�ȣ����ٽ�Ũ�ȣ��ⶨ�Ӷ�����������ʵ���������Zn+2H2SO4(Ũ)=ZnSO4+SO2��+2H2O�ķ���ʽ�����������һ�����Ķ���������Ҫ���ĵ����ᣬ����������ʵ�����ȥ����һ���������������ĵ���������ʵ����������ʣ����������ʵ���������c=![]() ����������ղⶨ������ٽ�Ũ�ȡ�
����������ղⶨ������ٽ�Ũ�ȡ�
��1���տ�ʼ�����Ũ�ȱȽϴ���п��Ӧ���ɶ��������䷴Ӧ����ʽΪZn+2H2SO4(Ũ)=ZnSO4+SO2��+2H2O��
��2����װ����һ�����巢��װ�ã�����װ����֮���װ�õ������ԣ������������ã��ټ���ҩƷ��
��3���÷�Ӧ�Ǹ����ȷ�Ӧ��������B�������ǵ��������������ã�ʹˮ������������������ȷ��������Һ�������������ã����û�������ƣ����ղⶨ���ٽ�Ũ�Ȼ�ƫ�ͣ�
��4��������������Ⱦ���岻���ŷŵ������У���Ҫ������������Һ���գ����ø����C��ֹҺ�巢���������ж������Ѵ��ٽ�Ũ��:���ݷ�Ӧһ��ʱ�䣬Ũ�����Ϊϡ���ᣬϡ������п��Ӧ�������ɶ�����������������������F���ռ����岢�鴿�����ȷ���ռ�����������֤������Ũ���Ѿ������ٽ�����£�
��5������������H2O2��Һ��������������Ϊ�����ƣ�����������BaCl2��Һ�������ᱵ��������ַ�Ӧ�����ó������ˡ�ϴ�ӡ���������õ���������Ϊa�ˣ�n(BaSO4)=![]() ��n(SO2)=
��n(SO2)=![]() ��������������ʵ���Ϊ��n(H2SO4) =n(SO2)=2��
��������������ʵ���Ϊ��n(H2SO4) =n(SO2)=2��![]() ��Zn+2H2SO4(Ũ)=ZnSO4+SO2��+2H2O��Ũ������п��Ӧ���ٽ�Ũ��Ϊ��
��Zn+2H2SO4(Ũ)=ZnSO4+SO2��+2H2O��Ũ������п��Ӧ���ٽ�Ũ��Ϊ��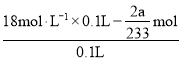 =
=
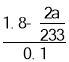 mol/L��
mol/L��
��6�������������ữ�ĸ��������Һ��D�е�SO32-���еζ�����Ϊ�ڵζ��Ĺ�������Һ�е�����������ӻᱻ�����е���������Ϊ��������ӣ���ɵζ������ȷ��

 ��У��ʦ������ҵ���Ӻ����Ծ�ϵ�д�
��У��ʦ������ҵ���Ӻ����Ծ�ϵ�д� ȫ�̽��ϵ�д�
ȫ�̽��ϵ�д�����Ŀ����![]() ��
��![]() ��
��![]() ������ȣ��ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������н��з�Ӧ��
������ȣ��ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������н��з�Ӧ��![]() ���õ������������ݣ�����ʵ��١���û��ʹ�ô���������˵������ȷ���ǣ� ��
���õ������������ݣ�����ʵ��١���û��ʹ�ô���������˵������ȷ���ǣ� ��
ʵ�� | �¶�/�� | ��ʼ | ƽ�� | ��ƽ������ʱ��/min |
�� | 500 | 5.00 | 2.00 | 40 |
�� | 800 | 3.00 | 1.00 | 15 |
�� | 500 | 3.00 | 1.20 | 9 |
A. ʵ����У���![]() �ڣ���
�ڣ���![]() ��ʾ�ķ�Ӧ���ʴ���
��ʾ�ķ�Ӧ���ʴ���![]()
B. �Ƚ�ʵ��ٺ͢ڣ�����˵��Ũ�ȶԷ�Ӧ���ʵ�Ӱ��
C. �Ƚ�ʵ��ٺ͢ڣ�����˵����Ӧ�������¶����߶�����
D. �Ƚ�ʵ��ںۣ͢�˵��ʵ���ʹ���˴���