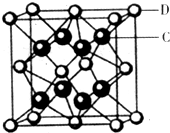
��Ŀ����
��ͼ�Dz��ֶ�����Ԫ�صij������ϼ���ԭ�������Ĺ�ϵͼ��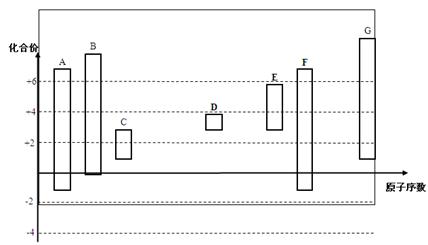
��1��Ԫ��A�����ڱ��е�λ�� ��
��2���õ���ʽ��ʾD2G���γɹ��� ��������ѧ������Ϊ ��
��3��C2-��D+��G2-���Ӱ뾶��С˳���� > > �������ӷ��Żش�
��4��ijͬѧ���ʵ��֤��A��B��F�ķǽ�����ǿ����ϵ�� 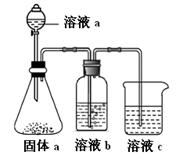
�� ��Һa��b�ֱ�Ϊ �� ��
�� ��Һc�е����ӷ���ʽΪ ��
�����ԭ�ӽṹ�ĽǶȽ��ͷǽ�����B > A��ԭ�� ��
��5����0.5 mol D2C2Ͷ��100 mL 3 mol/L ECl3��Һ��
�� ת�Ƶ��ӵ����ʵ���Ϊ ��
�� ��һ�����ӷ���ʽ��ʾ�÷�Ӧ ��
��1���ڶ����ڢ�A�壨1�֣�
��2�� ��1�֣� ���Ӽ���1�֣�
��1�֣� ���Ӽ���1�֣�
��3�� S2->O2->Na+ ��1�֣�
��4���� ���ᣨHNO3����1�֣� ����NaHCO3��Һ��1�֣�ȱ�١����͡������֣�
�� SiO2- 3+CO2+H2O=H2SiO3��+CO2- 3 (дH4SiO4Ҳ���֣���1�֣�
�� ̼�͵�Ԫ�ش���ͬһ���ڣ���ԭ�ӵ��˵��������̼ԭ�ӣ�ԭ�Ӱ뾶��̼ԭ��С����ԭ�Ӻ˶��������ӵ������������õ���������ǿ����˵�Ԫ�صķǽ�����ǿ��̼Ԫ�ء� ��2�֣�
��5����0.5 mol ��1�֣�
��10Na2O2 + 6Al3+ + 6H2O = 4Al(OH)3 + 2AlO��2+ 5O2��+ 20Na+ ��2�֣�
������������������������=�����������������=����������-8��F��O�����ۣ������ԭ��������֪��A��C��B��N��C��O��D��Na��E��Al��F��Si��G��S��
��1��Cλ�ڵڶ����ڢ�A��
��2��Na2S���γɹ��� ���������Ӽ���
���������Ӽ���
��3�� S2-��3�����Ӳ㣬O2-��Na+ֻ��2�����Ӳ㣨���Ӳ�ṹ��ͬ������Խ�뾶ԽС����
���ԣ�S2->O2->Na+ ��
��4���ǽ�����ǿ��������������ˮ���������ǿ���йأ�C��N��Si������������ˮ����ֱ�ΪH2CO3��HNO3��H2SiO3��������Һ��һ����ѭǿ���������ԭ����������ҺaΪHNO3������aΪNa2CO3����ҺbΪ����NaHCO3��Һ�����ڳ�ȥCO2�е�HNO3����ҺcΪNa2SiO3��
��5���ٵ���ת�Ʒ�����Na2O2�е�O��ÿ��Na2O2ת��1�����ӣ�����0.5 mol Na2O2ת�Ƶ���0.5 mol��
�ڷ�ӦΪ��10Na2O2 + 6Al3+ + 6H2O = 4Al(OH)3 + 2AlO��2+ 5O2��+ 20Na+
���㣺���Ԫ���ƶϿ���Ԫ�����ڱ����ɣ�������ʽ����ѧ����Ԫ�ؼ��仯����֪ʶ��������ԭ֪ʶ��

A��B��C��D��EΪǰ��������ԭ���������������Ԫ�أ���ص���Ϣ���£�
| Ԫ�� | �����Ϣ |
| A | AԪ��ԭ�Ӻ���ֻ�������ܼ�����ÿ���ܼ��Ϻ�����ȵĵ����� |
| B | �ǿ����к�����ḻ��Ԫ�� |
| C | �������У�����C�Ľ�������ǿ |
| D | ��̬ԭ�ӵ����ܲ�����7���˶�״̬��ͬ�ĵ��� |
| E | һ�ֺ��ص�������Ϊ63��������Ϊ34 |
���ö�Ӧ��Ԫ�ط��Żش��������⣺
��1��A������γ�һ�ֵķ���ʽΪA2H4������÷����д��ڦҼ���м���Ŀ��Ϊ ��
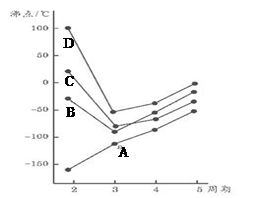
��2��H��A��H��B���ֹ��ۼ��У����ܽϴ���� ��H��A��H��D���ֹ��ۼ��У����ļ��Խ�ǿ����
��3��Eλ�����ڱ��е�λ���� ������E��B������������ˮ�����ϡ��Һ��Ӧ�����ӷ���ʽΪ ��
��4���������������仯ʾ��ͼ����д��BO��AO2��Ӧ���Ȼ�ѧ����ʽ ��

��5��C������������Ӧ��ˮ����ΪM��M�к��еĻ�ѧ������Ϊ ����һ������D2ͨ��һ��Ũ��M��ˮ��Һ�У�����ǡ����ȫ��Ӧʱ���������������ֺ�DԪ�ص����ӣ������������ӵ����ʵ�����n���뷴Ӧʱ�䣨t���ı仯ʾ��ͼ����ͼ��ʾ����д��t2ʱ���ܷ�Ӧ����ʽ
A��B��C��D��E��F��Ԫ�����ڱ�ǰ�����ڵ�����Ԫ�أ�ԭ���������������������Ϣ���±���
| Ԫ�� | �����Ϣ |
| A | ԭ�ӵĺ���������͵��Ӳ������ |
| B | ��̬ԭ�Ӽ۵����Ų�Ϊnsnnpn |
| C | ��̬�⻯��������������ˮ���ﷴӦ������ |
| D | ��̬ԭ�ӵ����Ų���2��δ�ɶԵ��� |
| E | λ�ڵ������ڣ���ͬ������ԭ�Ӱ뾶��� |
| F | ��B �γɵĺϽ�ΪĿǰ�������Ľ������� |
��1��Cλ��Ԫ�����ڱ��� ���ڵ� �塣FԪ�ػ�̬ԭ�ӵĺ�������Ų�ʽ�� ��
��2������Ԫ���У��縺������Ԫ���� ����Ԫ�ط��ţ���D��һ�ֺ���ԭ�Ӻ�����10�����ӣ��ú��صķ����� ��
��3��E2D2�ĵ���ʽ�� ��BD2�ľ�������Ϊ �����������D��F����Ԫ����ɣ������������һ�����ϣ������ﶡ��B��D����Ԫ����ɡ���ҵ���ɱ��Ͷ��ڸ����·�Ӧ����F�ĵ��ʣ�д���÷�Ӧ�Ļ�ѧ����ʽ�� ��
��4����2L�ܱ������м���3molA2��һ����C2������Ӧ��3A2+C2
 2CA3��H��0����Ӧ10min�ﵽƽ�⣬����0.2molCA3��
2CA3��H��0����Ӧ10min�ﵽƽ�⣬����0.2molCA3���ٸ÷�Ӧƽ�ⳣ������ʽΪ�������ʾ�д��ѧʽ��K��
�ڴ���ʼ��ƽ�⣬��C2Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ
X��Y��Z��W��Ԫ�����ڱ�ǰ�����ڳ���������Ԫ�أ�ԭ��������������X�ĵ��ʼ��ЦҼ��V�Цм�����X�ĵ�һ�����ܱ�������Ԫ�ض���Y�ĵ縺�Ա�X��С�����̬ԭ��������p�����Ǹò�s���ӵ�������Z��ǰ36��Ԫ����ԭ�Ӱ뾶��������Ԫ�أ�W��һ�ֺ��ص���������56����������30��
(1) Yλ��Ԫ�����ڱ���_______���ڵ�_______�壬W2+�ĺ�������Ų�ʽ��______��
(2) X��������XO2��H2O�Ƚϣ��۵�ϸߵ���_______ (�ѧʽ)��Z���⻯������ ���壬Z2O2�Ļ�ѧ��������_______(���ţ�
| A�����Ӽ� | B�����Թ��ۼ� | C���Ǽ��Թ��ۼ� | D�������� |
(4)��250C��101kPa�£�W�ĵ�����������ȼ�պ�ָ���ԭ�¶Ⱥ�ѹǿ��ƽ��ÿת��1mol���ӷų�QkJ����������W����ȼ�յ��Ȼ�ѧ����ʽ��_______��
�±���Ԫ�����ڱ�ǰ�����ڵ�һ���֣�X��Y��Z��R��W��J��6��Ԫ�صĴ��š�
| X | Y | Z | |
| | R | | |
| | | W | |
| | | | J |
��ش���������(���ر�˵���⣬���漰��Ԫ�ػش��������þ���Ԫ�ط��ű�ʾ)��
(1) �ڻ�����YZ2��Y�Ļ��ϼ�Ϊ________��Y2����Na���İ뾶��СΪ_______________��
(2) Rԭ�ӵĻ�̬�����Ų�ʽΪ
__________________________________________________________________________��
(3)��X��Y��Z����Ԫ���У���һ�������ɴ�С��˳����______________________��
(4)��һ����HX3����������������HX3��Һ��NaOH��Һ��Ӧ�����ӷ���ʽΪ___________________________________________��
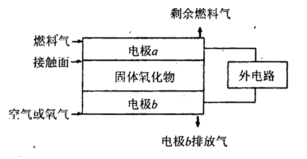
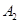 ��Ϊȼ��������Ӵ����Ϸ����ķ�ӦΪ______________________________��
��Ϊȼ��������Ӵ����Ϸ����ķ�ӦΪ______________________________��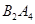 ��Ϊȼ��������Ӵ����Ϸ����ķ�ӦΪ________________________________��
��Ϊȼ��������Ӵ����Ϸ����ķ�ӦΪ________________________________��