题目内容
如图为四、五、六、七主族元素简单氢化物沸点随周期变化图像,(代表氢化A、B、C、D物中另外一种元素)分析图像并回答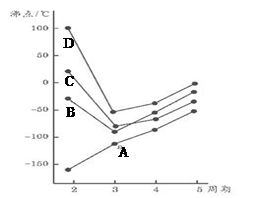
(1)写出B3-的空间构型
(2)B元素另外一种氢化物可做火箭的燃料,其电子式为:__________________,中心原子杂化方式为_______________
(3)A元素氧化物晶体类型为____________________,研究发现其氧化物晶胞中,A的位置与金刚石晶胞中碳原子位置相似,试分析晶胞中占有氧原子个数应为___________个。
(4)A、B、C、D第一电离能由小到大的顺序是____________________(用元素符号表示)
(1)直线形
(2) sp3杂化
sp3杂化
(3)原子晶体 16
(4)Si<O<N<F
解析试题分析:由图像和题意可知A、B、C、D分别为:SiH4、NH3、HF、H2O
(1)B3-为N3-故空间构型为直线形
(2)B元素另外一种氢化物可做火箭的燃料故为N2H4,电子式略、 sp3杂化
(3)A元素氧化物为SiO2故晶体类型为原子晶体; 其氧化物晶胞中,A的位置与金刚石晶胞中碳原子位置相似,故每个晶胞中占有的Si原子数为8,根据SiO2可知O原子数为16。
(4)根据第一电离能规律由小到大的顺序为Si<O<N<F
考点:考查原子结构、电离能、杂化轨道等相关知识。

 阅读快车系列答案
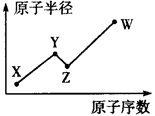
阅读快车系列答案X、Y、Z、M、Q、G六种短周期元素,原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,Y的一种同位素原子常用于测定文物的年代;Q形成的单质为淡黄色固体。请回答下列问题(涉及物质均用化学式表示)。
(1)离子化合物ZX中X离子的结构示意图为 ; Y在元素周期表中的位置是_______________。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是_______________,Q与G的气态氢化物还原性更强的是__________________。
(3)工业上制备M的高纯度单质,其中一个重要反应是:由MXG3与X2在高温下反应。该反应过程必须控制无水无氧,因为MXG3遇水剧烈反应生成H2、 和 ,而混入氧气,引起的后果是 。
(4)X2Q的燃烧热为a kJ·mol-1,下列X2Q燃烧反应的热化学方程式正确的是 。
| A.2X2Q(g) + O2(g) =" 2Q(s)" + 2X2O(g)△H=" -2a" kJ·mol-1 |
| B.X2Q(g) + 2O2(g) = QO3(g) + X2O(l)△H=" +a" kJ·mol-1 |
| C.2X2Q(g)+ 3O2(g) = 2QO2(g) + 2X2O(l)△H=" -2a" kJ·mol-1 |
| D.X2Q(g) + 2O2(g) = QO3(g) + X2O(l)△H=" -a" kJ·mol-1 |
 Fe + 2ZG 放电时,电池的正极反应式为: 该电池的电解质为___________________。
Fe + 2ZG 放电时,电池的正极反应式为: 该电池的电解质为___________________。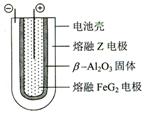
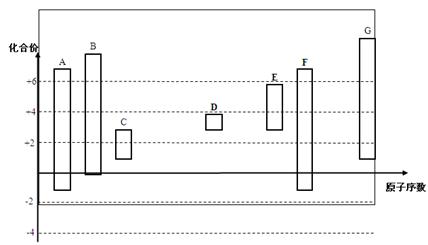
下图是元素周期表的一部分,其中每个数字编号代表对应的一种元素。
| ① | | | ||||||
| | | | | ② | ③ | ④ | | |
| ⑤ | | ⑥ | ⑦ | | | ⑧ | ⑨ | |
请按要求回答下列问题:
(1)画出元素②的原子结构示意图 。
(2)属于稀有气体的元素编号是_______,可作半导体材料的元素编号是______。
(3)③、⑦两种元素相比较,非金属性强的是 (填元素符号)。
(4)元素④的单质与元素⑤的单质反应可生成两种化合物,化学式分别是 , 。
(5)元素③和元素⑧的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可
看到大量的白烟,写出产生该现象的化学方程式: 。
 Si(s)+2CO(g)
Si(s)+2CO(g)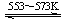 SiHCl3(l)+H2(g) + Q(Q>0)
SiHCl3(l)+H2(g) + Q(Q>0) Si(纯)+3HCl(g)
Si(纯)+3HCl(g)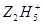 将Fe3+还原为Fe2+,
将Fe3+还原为Fe2+,