题目内容
17.下表为周期表的一部分,有关短周期X、Y、Z、R四种元素叙述正确的是( )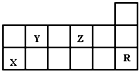
| A. | 热稳定性:Y的气态氢化物<Z的气态氢化物 | |
| B. | X的最高价氧化物对应水化物的酸性比Y的强 | |
| C. | X元素的单质能与所有强酸发生反应放出H2 | |
| D. | R元素的单质化学性质活泼 |
分析 由元素在周期表中的位置可知,R为Ar,则X为Al,Y为C,Z为O,结合元素及其单质、化合物的性质来解答.
解答 解:由元素在周期表中的位置可知,R为Ar,则X为Al,Y为C,Z为O,
A.非金属性越强,气态氢化物越稳定,则非金属性Z>Y,热稳定性为Y的气态氢化物<Z的气态氢化物,故A正确;
B.X为Al,其对应最高价氧化物的水化物为两性氢氧化物,酸性弱于碳酸,故B错误;
C.Al与浓硫酸和硝酸反应不能生成氢气,故C错误;
D.R为Ar,最外层电子数为8,不容易失去和得到电子,化学性质稳定,故D错误;
故选:A.
点评 本题考查位置、结构、性质的关系,明确元素在周期表中的位置及元素周期律是解答本题的关键,题目难度不大,注意稀有气体在周期表中的位置即可解答.

练习册系列答案
相关题目
8.已知反应A?2B,A、B的浓度变化如图所示,下列反应速率正确的是( )

| A. | v(A)=9 mol/(L•min) | B. | v(B)=18 mol/(L•min) | ||
| C. | v(A)=4.5 mol/(L•min) | D. | v(B)=4.5 mol/(L•min) |
5.化学与能源开发、环境保护、资源利用等密切相关.下列说法正确的是( )
| A. | 为提高农作物的产量和质量,应大量使用化肥和农药 | |
| B. | 光缆在信息产业中有广泛应用,制造光缆的主要材料是单质硅 | |
| C. | 实现化石燃料清洁利用,就无需开发新能源 | |
| D. | 垃圾是放错地方的资源,应分类回收利用 |
2.物质M的结构式如图所示,常被用于香料或作为饮料的酸化剂.下列关于物质M的说法正确的是( )

| A. | M分子式为C6H6O7 | |
| B. | 1 mol物质M可以和3 mol氢气发生加成 | |
| C. | M分子不可以发生消除反应 | |
| D. | 足量的M分别与等物质的量的NaHCO3、Na2CO3反应得到的气体物质的量相同 |
9.下列变化中,不需要破坏化学键的是( )
| A. | 氯化氢溶于水 | B. | 加热氯酸钾使其分解 | ||
| C. | 干冰升华 | D. | 二氧化硅熔化 |
6.已知:H2(g)+F2(g)═2HF(g);△H=-270kJ/mol,下列说法正确的是( )
| A. | 氟化氢气体分解生成氢气和氟气的反应是放热反应 | |
| B. | 1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于270 kJ | |
| C. | 在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量 | |
| D. | 该反应中的能量变化可用如图来表示 |
7. 火力发电厂产生的烟气中含有CO2、CO、SO2等物质,直接排放会对环境造成危害.对烟气中CO2、CO、SO2等物质进行回收利用意义重大.
火力发电厂产生的烟气中含有CO2、CO、SO2等物质,直接排放会对环境造成危害.对烟气中CO2、CO、SO2等物质进行回收利用意义重大.
(1)“湿式吸收法”利用吸收剂与烟气中的SO2发生反应从而脱硫,其中“钠碱法”用NaOH溶液作吸收剂,向100mL2mol•L-1的NaOH溶液中通入标准状况下4.48LSO2气体,反应后测得溶液pH<7.则溶液中下列各离子浓度关系正确的是abd(填字母序号).
a.c(HSO3-)>c(SO32-)>c(H2SO3)
b.c(Na+)>c(HSO3-)>c(H+)>c(SO32-)
c.c(Na+)+c(H+)=c(HSO3-)+c(SO32-)+c(OH-)
d.c(H+)=c(SO32-)-c(H2SO3)+c(OH-)
(2)工业上常用高浓度的K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如图所示:
①在阳极区发生的反应中的非氧化还原反应的离子方程式为4OH--4e-═2H2O+O2↑.
②简述CO32-在阴极区再生的原理HCO3-存在电离平衡:HCO3-?H++CO32-,阴极H+放电浓度减小,平衡右移,CO32-再生;阴极H+放电OH-浓度增大,OH-与HCO3-反应生成CO32-,CO32-再生.
(3)下表中列出了25℃、l0l kPa时一些物质的燃烧热数据:
已知键能:C-H键:413.4kJ.mol-l.H-H键:436.0kJ•mol-1,请计算:
①2CH4(g)=C2H2(g)+3H2(g)△H=376.4 kJ•mol-1
②C2H2中-C≡C-的键能为796.0 kJ/molkJ•mol-l
(4)熔融盐燃料电池是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极.负极反应式为CH4+4CO32--8e-=5CO2+2H2O.
为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,为此电池工作时必须有部分A物质参加循环,则A物质的化学式是CO2.
 火力发电厂产生的烟气中含有CO2、CO、SO2等物质,直接排放会对环境造成危害.对烟气中CO2、CO、SO2等物质进行回收利用意义重大.
火力发电厂产生的烟气中含有CO2、CO、SO2等物质,直接排放会对环境造成危害.对烟气中CO2、CO、SO2等物质进行回收利用意义重大.(1)“湿式吸收法”利用吸收剂与烟气中的SO2发生反应从而脱硫,其中“钠碱法”用NaOH溶液作吸收剂,向100mL2mol•L-1的NaOH溶液中通入标准状况下4.48LSO2气体,反应后测得溶液pH<7.则溶液中下列各离子浓度关系正确的是abd(填字母序号).
a.c(HSO3-)>c(SO32-)>c(H2SO3)
b.c(Na+)>c(HSO3-)>c(H+)>c(SO32-)
c.c(Na+)+c(H+)=c(HSO3-)+c(SO32-)+c(OH-)
d.c(H+)=c(SO32-)-c(H2SO3)+c(OH-)
(2)工业上常用高浓度的K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如图所示:
①在阳极区发生的反应中的非氧化还原反应的离子方程式为4OH--4e-═2H2O+O2↑.
②简述CO32-在阴极区再生的原理HCO3-存在电离平衡:HCO3-?H++CO32-,阴极H+放电浓度减小,平衡右移,CO32-再生;阴极H+放电OH-浓度增大,OH-与HCO3-反应生成CO32-,CO32-再生.
(3)下表中列出了25℃、l0l kPa时一些物质的燃烧热数据:
| 物质 | CH4 | C2H2 | H2 |
| 燃烧热/kJ•mol-1 | 890.3 | 1299.6 | 285.8 |
①2CH4(g)=C2H2(g)+3H2(g)△H=376.4 kJ•mol-1
②C2H2中-C≡C-的键能为796.0 kJ/molkJ•mol-l
(4)熔融盐燃料电池是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极.负极反应式为CH4+4CO32--8e-=5CO2+2H2O.
为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,为此电池工作时必须有部分A物质参加循环,则A物质的化学式是CO2.
 氧(O)、硫(S)、硒(Se)、碲(Te)为ⅥA族元素,请回答下列问题:
氧(O)、硫(S)、硒(Se)、碲(Te)为ⅥA族元素,请回答下列问题: 的沸点比
的沸点比 高,原因是对羟基苯甲醛分子间能形成氢键、邻羟基苯甲醛分子内能形成氢键.
高,原因是对羟基苯甲醛分子间能形成氢键、邻羟基苯甲醛分子内能形成氢键.

 .
.