题目内容
6.已知:H2(g)+F2(g)═2HF(g);△H=-270kJ/mol,下列说法正确的是( )| A. | 氟化氢气体分解生成氢气和氟气的反应是放热反应 | |
| B. | 1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于270 kJ | |
| C. | 在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量 | |
| D. | 该反应中的能量变化可用如图来表示 |
分析 A、放热反应的逆反应是吸热反应;
B、气体转化为液体的过程是一个放热过程,所以生成液态产物比生成气态产物放出热量多;
C、放热反应,反应物的能量总和大于生成物的能量总和;
D、放热反应,反应物的能量总和大于生成物的能量总和,所以生成物能量之和低;
解答 解:A、已知:H2(g)+F2(g)═2HF(g)△H=-270kJ/mol,放热反应的逆反应是一个吸热反应,所以氟化氢气体分解生成氢气和氟气的反应是吸热反应,故A错误;
B、HF气体转化为液态HF的过程是一个放热过程,所以1molH2与1molF2反应生成2 mol液态HF放出的热量大于270kJ,故B错误;
C、已知:H2(g)+F2(g)═2HF(g)△H=-270kJ/mol,所以反应物的能量总和大于生成物的能量总和,即1molH2与1molF2的能量总和大于2molHF气体的能量,故C正确;
D、1molH2与1molF2的能量总和大于2molHF气体的能量,故D错误.
故选C.
点评 本题考查学生反应焓变的意义以及反应的吸放热和反应物、生成物能量总和之间的关系知识,难度不大.

练习册系列答案
相关题目
16.Mg3N2与水反应的化学方程式为Mg3N2+6H2O═3Mg(OH)2+2NH3↑,下列说法错误的是( )
| A. | 上述反应中,有两种离子化合物 | |
| B. | Mg3N2中,N3-的半径比Mg2+的半径大 | |
| C. | H2O与NH3含有相同的电子数,但H2O比NH3的稳定性差 | |
| D. | 碱性:Mg(OH)2>Al(OH)3 |
17.下表为周期表的一部分,有关短周期X、Y、Z、R四种元素叙述正确的是( )
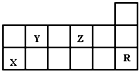

| A. | 热稳定性:Y的气态氢化物<Z的气态氢化物 | |
| B. | X的最高价氧化物对应水化物的酸性比Y的强 | |
| C. | X元素的单质能与所有强酸发生反应放出H2 | |
| D. | R元素的单质化学性质活泼 |
1.下列对于加成反应的说法中正确的是( )
| A. | 加成反应的结果是使有机化合物中不再含有不饱和键 | |
| B. | 福尔马林可以作为食品保鲜剂 | |
| C. | 甲苯在光照条件下与氯气反应,主要生成2,4-二氯甲苯 | |
| D. | 等物质的量的苯与苯甲酸完全燃烧消耗氧气的量相等 |
11.下列化学用语书写正确的是( )
| A. | 氯原子的结构示意图: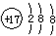 | |
| B. | N2的电子式: | |
| C. | CH4分子的比例模型: | |
| D. | 用电子式表示氯化氢分子的形成过程: |
18.下列过程能实现热能转化为化学能的是( )
| A. | HCl十NaOH=NaCl十H2O | B. | 碳酸钙受热分解 | ||
| C. | 镁条溶于盐酸 | D. | CaO十H2O=Ca(OH)2 |
15.反应A+3B═2C+2D 在四种不同条件下的反应速率为:( )
(1)v(A)=0.3mol/(L•s )
(2)v(B)=0.6mol/(L•s)
(3)v(C)=0.4mol/(L•s)
(4)v(D)=0.45mol/(L•s)
(1)v(A)=0.3mol/(L•s )
(2)v(B)=0.6mol/(L•s)
(3)v(C)=0.4mol/(L•s)
(4)v(D)=0.45mol/(L•s)
| A. | (4)>(1)>(2)=(3) | B. | (2)>(1)>(4)=(3) | C. | (1)>(4)>(2)=(3) | D. | (3)>(4)>(2)=(1) |
16.下列各项中表达正确的是( )
| A. | N2的结构式::N≡N: | B. | F-离子结构示意图: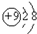 | ||
| C. | 用电子式表示HCl形成过程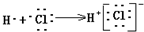 | D. | 次氯酸电子式 |

 (写结构简式).
(写结构简式). .
. 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).