��Ŀ����
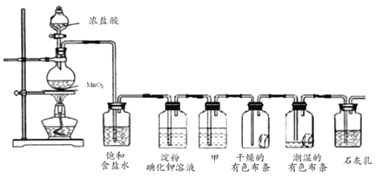
����Ŀ����.ʵ���Ҿ���Ҫ��ȡij�����岢��֤����������ʡ�
��1������װ���ʺ���β�����յ���________������ţ���
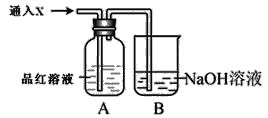
��2��������װ����ͨ������X��A��Ʒ����Һ��ɫ����X������_____�����������֣����Ҫ֤��X��SO2����,�������IJ�����______
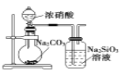
��.ʵ������FeSO4��Һ��NaOH��Һ��Ӧ��ȡFe(OH)2��ȴ���ѿ����ȶ��İ�ɫ��������ͬѧ�����һ���µ�ʵ�鷽����������������ɰ�ɫ��������ɫ����ת���ɺ��ɫ������������������¿հף�
��1��ȡһ�������0.1mol.L-1NaOH��Һ�����ձ��У�______���ٵ��뼸��ֲ���ͣ�
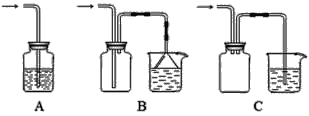
��2��ѡ��װ��_______��������������������������1��������Һ���뵽װ���в���ͼʾ��װ��װ�á�
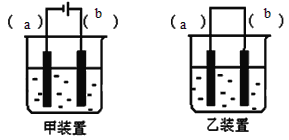
��3������ѡ���װ���ϱ����缫���Ϸֱ�Ϊ__________��________
��4��ʵ���п���______�����ȶ��İ�ɫFe(OH)2������
��5�����Ҫ������ɫ����ת��Ϊ���ɫ�����ĵ����������IJ�����________
���𰸡���.��1��BC��2�֣�
��2��SO2��Cl2��O3��ClO2�ȣ���2�֣�����ɫ�����Һ�ټ��ȣ������Һ�ָֻ��ɺ�ɫ����Xһ��ΪSO2��2�֣�
��.��1��������У�2�֣�
��2��װ�ü� ��2�֣�
��3��b-Fe ��1�֣� a-ʯī��Fe�� ��1�֣�
��4������������Һ�� ��2�֣�
��5�����缫�������� ��2�֣�
��������
����
��.��1���������Ҫ�ӷ�ֹ�����ĽǶ�ȥ�롣
��2����ʹƷ����ɫ�Ŀ������뵽SO2����ϸ��һ�»���Cl2��O3��ClO2�����Ҫ֤��ͨ����Ƕ���������Ҫ���Թ�ȡ��ɫ�����Һ���þƾ��ƽ��м��ȣ����Ƿ��ָܻ���ɫ���������ʱһ��Ҫ�в�����������
��.����Ҫע��Ŀ��Ϊ���Ʊ�Fe(OH)2���۲�����ɫ�����Թؼ������õ��Լ�Ҫ��O2��װ��Ҫ������������1����ҺҪ���������ü�����еķ������¶����ߣ�������ˮ�ǵ��ܽ���½���2������װ�õ���������������ӵ�Դ�����������Ƕ�ѡһ������������ü���ѡ��һװ�ã��������⣻�ӱ���ĽǶȣ���֪Ҫ�������������ӣ��ٺ����������ӷ�Ӧ������Ҫѡ�õ��أ�����װ�ã�b�缫Ϊ��������������������ΪFe��a�缫Ϊʯī����Ϊ�����ϲ������������ӣ�����ɫ�����������ĸ����ɹ۲쵽�����Ҫ���ɫ����ת��Ϊ���ɫ��������Ҫ�������������������в��ܼ��룬��������缫���ӣ��൱���ö��Ե缫�������������Һ�������ˮ�������Ϳɲ����ˣ�Ҳ��ʵ����ת����

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ������ʵ���������������Ӧ����
A | B | C | D | |
ʵ�� |
|
|
|
|
���� | ������ָ������ƫ��������Feת�Ƶ�Cu����Ƭ�̺�����ƫ | ����һ��ʱ�����Һ��ɫ��ȥ | ���ȣ�����Һ�в�����ɫ���� | ��ƿ���д�������ð����Na2SiO3��Һ����� |
���� | ��Ƭ��������Ƭ�̺�ͭƬ������ | ����������������ˮ�⣬������������ | ������ˮ������Ӧ����H2 | �ǽ����ԣ� N��C��Si |
A.AB.BC.CD.D