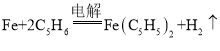题目内容
【题目】下列实验的现象与结论相对应的是
A | B | C | D | |
实验 |
|
|
|
|
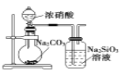
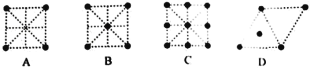
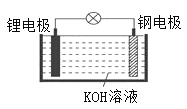
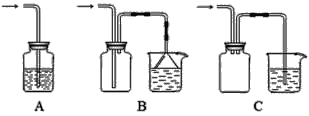
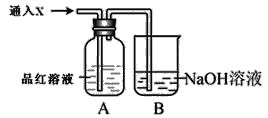
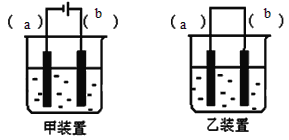
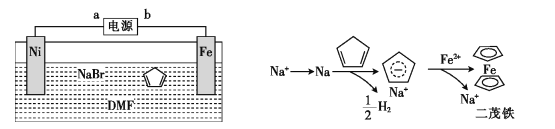
现象 | 电流计指针向右偏(电子由Fe转移到Cu),片刻后向左偏 | 加热一段时间后溶液蓝色褪去 | 加热,肥皂液中产生无色气泡 | 烧瓶中有大量气泡冒出,Na2SiO3溶液变浑浊 |
结论 | 铁片作负极,片刻后铜片作负极 | 淀粉在酸性条件下水解,产物是葡萄糖 | 铁粉与水蒸气反应生成H2 | 非金属性: N>C>Si |
A.AB.BC.CD.D
【答案】A
【解析】
A.常温下Fe遇浓硝酸发生钝化,片刻后Cu与浓硝酸反应,则开始时Fe为负极,片刻后Fe为正极,可观察到电流计指针向右偏(电子由Fe转移到Cu),片刻后向左偏,故A正确;
B.淀粉遇碘单质变蓝,实验没有检验葡萄糖,则图中实验不能确定淀粉的水解产物,故B错误;
C.应点燃肥皂泡,试管中有空气也产生气泡,则由产生无色气泡不能确定生成氢气,故C错误;
D.浓硝酸易挥发,硝酸与硅酸钠反应,则图中实验不能比较碳酸、硅酸的酸性,则不能比较非金属性,故D错误;
故答案选A。

练习册系列答案
 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目