��Ŀ����
��Ԫ�صĻ����������������������Ź㷺��Ӧ�á�
��1��400�棬1.01��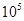 Pa�£��ݻ�Ϊ1��0L���ܱ������г���0.5molSO2, (g)��0.3 molO2 (g)��������Ӧ2SO2(g)��O2(g)
Pa�£��ݻ�Ϊ1��0L���ܱ������г���0.5molSO2, (g)��0.3 molO2 (g)��������Ӧ2SO2(g)��O2(g) 2SO3(g) ��H����198kJ/mol����Ӧ��n(SO3)��n(O2)��ʱ��仯�Ĺ�ϵ����ͼ��ʾ
2SO3(g) ��H����198kJ/mol����Ӧ��n(SO3)��n(O2)��ʱ��仯�Ĺ�ϵ����ͼ��ʾ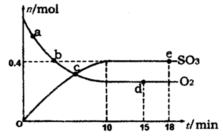 ����Ӧ��ƽ�ⳣ��K��_______��0��10 min����SO2��ʾ��ƽ����Ӧ����_________������ͼ����Ϣ���ж�������������ȷ����_____������ţ���
����Ӧ��ƽ�ⳣ��K��_______��0��10 min����SO2��ʾ��ƽ����Ӧ����_________������ͼ����Ϣ���ж�������������ȷ����_____������ţ���
| A��a��ʱ�̵�����Ӧ���ʱ�b��ʱ�̵Ĵ� |
| B��c��ʱ�̷�Ӧ�ﵽƽ��״̬ |
| C��d���e��ʱ�̵�c(O2)��ͬ |
| D����5 00�棬1.01��105Pa�£���Ӧ�ﵽƽ��ʱ��n( SO3) ��ͼ��e��ʱ�̵�ֵ�� |
��3����ͨ����ⷨʹ��2���е�����Һ������ѭ�����ã��缫��Ϊʯī�缫�����乤��ʾ��ͼ���£�
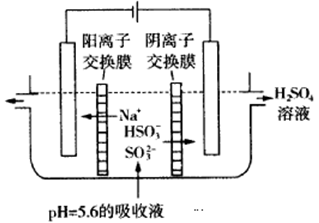
HSO3���������ҷ�Ӧ�ĵ缫��ӦʽΪ________________________�������ҵIJ���_________________��
����12�֣���1����6�֣�160 ��mol��L-1��-1��2�֣��� 0.04 mol��L-1��min-1��2�֣���AC��2�֣�
��2����2�֣�c(Na+)��c(HSO3-)��c(H+)��c(SO32-)
��3����4�֣�HSO3-+H2O��2e����SO42-+3H+��2�֣� H2��NaOH��2�֣�
���������������1������ͼ���֪����Ӧ���е�10minʱ��Ӧ�ﵽƽ��״̬��ƽ��ʱ������������ʵ�����0.4mol����Ũ����0.4mol/L����
2SO2(g)��O2(g) 2SO3(g)
2SO3(g)
��ʼŨ�ȣ�mol/L�� 0.5 0.3 0
ת��Ũ�ȣ�mol/L�� 0.4 0.2 0.4
ת��Ũ�ȣ�mol/L�� 0.1 0.1 0.4
���Ը÷�Ӧ��ƽ�ⳣ��K��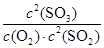 ��
��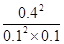 ��160
��160
0��10 min����SO2��ʾ��ƽ����Ӧ����0.4mol/L��10min��0.04 mol��L-1��min-1��
A��a��ʱ�̷�Ӧ���Ũ�ȴ���b��ʱ�̷�Ӧ���Ũ�ȣ�����a��ʱ�̵�����Ӧ���ʱ�b��ʱ�̵Ĵ�A��ȷ��
B��c��ʱ�����淴Ӧ���ʲ���ȣ����Է�Ӧû�дﵽƽ��״̬��B����ȷ��
C��d���e��ʱ�̵�ƽ��״̬������ͬ�ģ�����c(O2)��ͬ��C��ȷ��
D������Ӧ�Ƿ��ȷ�Ӧ�����������¶�ƽ�����淴Ӧ�����ƶ���������5 00�棬1.01��105Pa�£���Ӧ�ﵽƽ��ʱ��n( SO3) ��ͼ��e��ʱ�̵�ֵС��D����ȷ����ѡAC��
��2��������Һʧȥ��������ʱ����Ӧ���������������ơ�25��ʱ�����Һ��pH��5.6����˵��HSO3���ĵ���̶ȴ���HSO3����ˮ��̶ȣ�������Һ��Na��,H��, HSO3��,SO32�����ӵ�Ũ���ɴ�С��˳����c(Na+)��c(HSO3-)��c(H+)��c(SO32-)��
��3����������ʧȥ���ӣ�����������Ӧ�������õ����ӣ�������ԭ��Ӧ������HSO3���������ҷ�Ӧ�ĵ缫��ӦʽΪHSO3-+H2O��2e����SO42-+3H+����������Һ�е������ӵõ����ӣ�����������ͬʱ�ƻ�������Χˮ�ĵ���ƽ�⣬���������������������������ơ�
���㣺�������ƽ�ⳣ���ͷ�Ӧ���ʵ��йؼ��㣻ƽ��״̬�Լ����������ƽ��״̬��Ӱ�죻��Һ������Ũ�ȴ�С�Ƚ��Լ��绯ѧԭ�����й��жϺ�Ӧ�õ�

 ��У����ϵ�д�
��У����ϵ�д�ij������ȤС���H2O2�ķֽ�������������ʵ��̽����
�� �±��Ǹ�С���о�Ӱ��������⣨H2O2���ֽ����ʵ�����ʱ�ɼ���һ�����ݣ�
��10mL H2O2��ȡ150mLO2�����ʱ�䣨�룩
�� ��С������Ʒ���ʱ��������Ũ�ȡ�a: ��b: �����ضԹ�������ֽ����ʵ�Ӱ�졣
�� ������Ӱ��H2O2�ֽ����ʵ�����a��b����ѡһ����˵�������ضԸ÷�Ӧ���ʵ�Ӱ�죺
��
�� ��������ͬ���ۼ�״̬��ͬ��MnO2�ֱ���뵽5mL 5%��˫��ˮ�У����ô����ǵ�ľ
�����ԡ��ⶨ������£�
| ������MnO2�� | ������� | �۲��� | ��Ӧ��������ʱ�� |
| ��ĩ״ | ��ϲ��� | ���ҷ�Ӧ�������ǵ�ľ����ȼ | 3.5���� |
| ��״ | ��Ӧ���������Ǻ�����ľ��δ��ȼ | 30���� |
�� д��H2O2�����Ļ�ѧ��Ӧ����ʽ _______________ ______��
�� ʵ����˵���������õĴ�С��________ _________�йء�
̼���������ĵ��ʼ��仯�����ڹ�ũҵ����������������Ҫ�����á�
��1�����̼�Ȼ�ԭ���Ȼ�����ʵ���������Ʊ�������������ص��Ȼ�ѧ����ʽ���£�
2Al2O3(s)��2AlCl3(g)��6C(s)=6AlCl(g)��6CO(g) ��H��a kJ��mol��1
3AlCl(g) ��2Al(l)��AlCl3(g) ��H��b kJ��mol��1
��ӦAl2O3(s)��3C(s)��2Al(l)��3CO(g)�ġ�H= kJ��mol��1���ú�a��b�Ĵ���ʽ��ʾ����
��2���û���̿��ԭ�����Դ����������ij�о�С����ij�ܱ������м���һ�����Ļ���̿��NO��������ӦC(s)+2NO(g) N2(g)+CO2(g) ��H="Q" kJ��mol��1��T1��ʱ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�
N2(g)+CO2(g) ��H="Q" kJ��mol��1��T1��ʱ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�
| ʱ�䣨mol/L�� Ũ�ȣ�mol/L�� | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
��30min��ֻ�ı�ijһ��������Ӧ���´ﵽƽ�⣬�����ϱ��е������жϸı������������ ������ĸ��ţ���
a��ͨ��һ������NO b������һ�����Ļ���̿
c��������ʵĴ��� d���ʵ���С���������
����30min�������¶���T2�棬�ﵽƽ��ʱ��������NO��N2��CO2��Ũ��֮��Ϊ3��1��1����Q 0���>����<������
���ں��������£����жϸ÷�Ӧһ���ﵽ��ѧƽ��״̬�������� ����ѡ���ţ���
a����λʱ��������2n mol NO(g)��ͬʱ����n mol CO2(g)
b����Ӧ��ϵ���¶Ȳ��ٷ����ı�
c�����������ܶȲ��ٷ����ı�
d����Ӧ��ϵ��ѹǿ���ٷ����ı�
��3�������������Խ��Al��Ag2O��ؿ�����ˮ�¶�����Դ����ԭ������ͼ��ʾ��
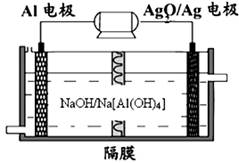
��д���õ��������Ӧʽ �������£��øû�ѧ��Դ�Ͷ��Ե缫���300ml����ͭ��Һ��������������27mg Al���������Һ��pH�� ����������Һ����ı仯����
�״�����Ϊ2l���͵�����ȼ�ϣ���ҵ��ͨ�����з�Ӧ��͢���CH4��H2OΪԭ�����Ʊ��״���
CH4(g)+H2O(g) CO(g)+3H2(g)������ CO(g)+2H2(g)
CO(g)+3H2(g)������ CO(g)+2H2(g) CH3OH(g) ������
CH3OH(g) ������
��1����1.0 mol CH4��2.0 mol H2O(g)ͨ���ݻ�Ϊ100L��Ӧ�ң���һ�������·�����ӦI��CH4��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��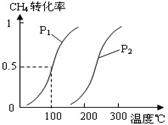
����֪100��ʱ�ﵽƽ�������ʱ��Ϊ5min������H2��ʾ��ƽ����Ӧ����Ϊ ��
��ͼ�е�P1 P2���<������>����=������100��ʱƽ�ⳣ����ֵΪ ��
��2����ѹǿΪ0.1 MPa������, ��a mol CO�� 3a mol H2�Ļ�������ڴ��������£��Է���Ӧ�����ɼ״���
�۸÷�Ӧ�ġ�H 0���������ݻ����䣬���д�ʩ�����Ӽ״����ʵ��� ��
| A�������¶� | B����CH3OH(g)����ϵ�з��� |
| C������He��ʹ��ϵ��ѹǿ���� | D���ٳ���1mol CO��3mol H2 |
| ʵ���� | T(��) | n(CO)/n(H2) | P��Mpa�� |
| i | 150 | 1/3 | 0.1 |
| ii | | | 5 |
| iii | 350 | | 5 |
a�������ϱ��ո�������ʣ���ʵ���������ݡ�
b�����ݷ�Ӧ����ص㣬�ڸ���������ͼ�У���������5MPa������CO��ת�������¶ȱ仯����������ʾ��ͼ��������ѹǿ��
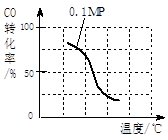
��ҵ�ϡ��̶���������CO2����Ч�ؼ��ᡰ���ҡ�ЧӦ����һ����CO2�����״�ȼ�ϵķ�����CO2(g)��3H2(g) CH3OH(g)��H2O(g) ��H =��49.0 kJ��mol��1
CH3OH(g)��H2O(g) ��H =��49.0 kJ��mol��1
��1������ͬ�¶Ⱥ��ݻ�����ʱ����˵���÷�Ӧ�Ѵ�ƽ��״̬������
| A��n(CO2)��n(H2)��n(CH3OH)��n(H2O)��1��3��1��1 |
| B��������ѹǿ���ֲ��� |
| C��H2������������CH3OH����������֮��Ϊ3��1 |
| D�������ڵ��ܶȱ��ֲ��� |
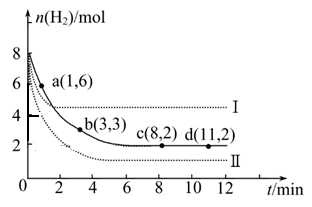
�� a������Ӧ���������淴Ӧ����(����ڡ��������ڡ���С�ڡ�)��
�� ���ı�ijһʵ������ʱ�����H2�����ʵ�����ʱ��仯��ͼ��������ʾ�����ߢ��Ӧ��ʵ�������ı����� �����ߢ��Ӧ��ʵ�������ı����� �� ����
�� �����ͼ�л�����������Ӧ�����ߡ�
�� ���ͼ��ʵ�ߵ����ݣ�������¶�ʱ��Ӧ�Ļ�ѧƽ�ⳣ������д��������̣�
��3���״���������ȼ�ϵ�أ�����KOH���������Һ�������ĵ缫��ӦʽΪ�� ��
ij��ѧʵ��С���ͬѧ������������װ������ȫ��ͬ��װ�ö���̽��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�졣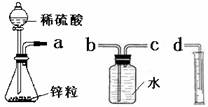
��1��Ϊ�ﵽ��ʵ��Ŀ����װ������˳��Ϊ��a��________��________��________.
��2�����Ӻ�װ�ú����һ��������
��3����ƿ�з�����Ӧ�����ӷ���ʽΪ
��4������װ�õķ�Һ©����װ���Լ��ֱ�Ϊ1mol/L�����4mol/L����,��С��ͬѧҪ�ⶨ����¼���������±���
| ������Լ� | H2���������ͬ�����£� | ��Ӧʱ�� | ��Ӧ���� |
| 1mol/L������ | 10mL | t1 | v1 |
| 4mol/L���� | 10mL | t2 | v2 |
��5������һ��ͬѧ�ⶨ��ÿ��һ���ӣ���ƿ�������Ũ�ȣ���¼������£�

���ڸ���������ͼ������v(H2)-t��ͼ��.
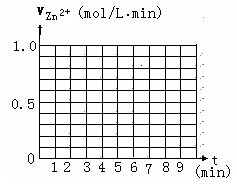
�����0��4mimʱ�û�ѧ��Ӧ������ʱ��仯��ԭ�� .
��6��������ʵ�鷽���ɶ����ⶨ�÷�Ӧ�Ļ�ѧ��Ӧ�����⣬�������е�ʵ��ⶨ�����У� ����дһ�֣�.
 2SO3(g)��
2SO3(g)��

 CO2(g)��H2(g)
CO2(g)��H2(g)