��Ŀ����
��ҵ�ϡ��̶���������CO2����Ч�ؼ��ᡰ���ҡ�ЧӦ����һ����CO2�����״�ȼ�ϵķ�����CO2(g)��3H2(g) CH3OH(g)��H2O(g) ��H =��49.0 kJ��mol��1
CH3OH(g)��H2O(g) ��H =��49.0 kJ��mol��1
��1������ͬ�¶Ⱥ��ݻ�����ʱ����˵���÷�Ӧ�Ѵ�ƽ��״̬������
| A��n(CO2)��n(H2)��n(CH3OH)��n(H2O)��1��3��1��1 |
| B��������ѹǿ���ֲ��� |
| C��H2������������CH3OH����������֮��Ϊ3��1 |
| D�������ڵ��ܶȱ��ֲ��� |
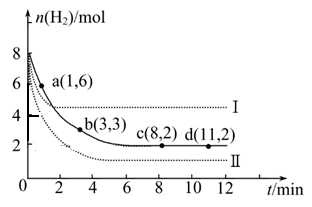
�� a������Ӧ���������淴Ӧ����(����ڡ��������ڡ���С�ڡ�)��
�� ���ı�ijһʵ������ʱ�����H2�����ʵ�����ʱ��仯��ͼ��������ʾ�����ߢ��Ӧ��ʵ�������ı����� �����ߢ��Ӧ��ʵ�������ı����� �� ����
�� �����ͼ�л�����������Ӧ�����ߡ�
�� ���ͼ��ʵ�ߵ����ݣ�������¶�ʱ��Ӧ�Ļ�ѧƽ�ⳣ������д��������̣�
��3���״���������ȼ�ϵ�أ�����KOH���������Һ�������ĵ缫��ӦʽΪ�� ��
��16�֣�
��1��BC��3�֣�ֻѡB��C��1�֣�ȫ�Ե�3�֣��������д��𰸲��÷֣�
��2���� ���ڣ�1�֣� �� �����¶� ��2�֣� ����ѹǿ��2�֣�
��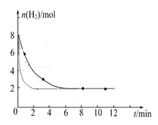 ��2�֣�
��2�֣�
��K=0.5L2 ?mol��2��������̼�������
������ʽ��ȷ��1�֣�ƽ�ⳣ������ʽ1�֣�����λ����ʽ1�֣�����������λ1�֣�
��3��CH3OH+8OH����6e��=CO32��+ 6H2O�� 2�֣�δ��ƽ��1�֣�
���������������1������ֱ仯�����ʵ���֮�ȵ��ڻ�ѧ����ʽ�е�ϵ��֮�ȣ�ƽ��ʱ���ʵ���֮�Ȳ�һ������ϵ��֮�ȣ���Aѡ���������Ӧ���������ʵ�����С�ķ�����˴�����Ӧ��ʼ����ʱ���������������ʵ�����С��ѹǿ��С����ѹǿ���ֲ��䣬˵�������ܵ����ʵ������ֲ��䣬��Ӧ�Ѵ�ƽ�⣬��Bѡ����ȷ�������Ƿ�Ӧ�����������Ϊv��(H2)���״������������������Ϊv��(CH3OH)������֮�ȵ��ڻ�ѧ����ʽ����Ӧ��ϵ��֮�ȣ�˵����Ӧ�Ѵ�ƽ�⣬��Cѡ����ȷ������ֶ������壬�����������������������������������ֲ��䣬���������������ܶ�ʼ�ղ��䣬����˵����Ӧ�Ѵ�ƽ�⣬��Dѡ�����2���������Ƿ�Ӧ�������Ӧ��ʼ����ʱ�������ʵ�����С��a���ʾ���������ʵ�����û�дﵽ���ޣ����ܼ�����С��˵����ʱ��Ӧ����������Ӧ������У�����v��(H2)> v��(H2)���ڶ�ͼ�ɵã�����I�ȴﵽƽ�⣬��ƽ��ʱ���������ʵ�����ԭƽ���˵����ȡ��������������Ӧ���ʣ�����ʹƽ�����淴Ӧ�����ƶ���������������Է�Ӧ���ʺ�ƽ���ƶ���Ӱ������ƶϣ�ֻ�������¶Ȳ��ܵõ�����I����Ϊ����Ӧ�Ƿ��ȷ�Ӧ��ֻ������ѹǿ���ܵõ�����II����Ϊ����Ӧ�����������С�ķ���������Ϊ�д�����ֻ�ܼӿ췴Ӧ���ʣ����̴ﵽƽ���ʱ�䣬����ʹƽ���ƶ������ܸı�������ʼʱ��ƽ��ʱ�����ʵ������ɴ˿��Ի����������ʱ���������ʵ����淴Ӧʱ��仯��ʾ��ͼ����������Ҫ�ı�ע�������������ݷ��Ͷ���ʽ��ƽ�ⳣ������
CO2(g)��3H2(g) CH3OH(g)��H2O(g)
CH3OH(g)��H2O(g)
��ʼŨ��/mol?L��1 3 4 0 0
�仯Ũ��/mol?L��1 1 3 1 1
ƽ��Ũ��/mol?L��1 2 1 1 1��2�֣�
K=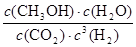 =
=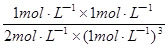 =0.5L2 ?mol��2��
=0.5L2 ?mol��2��
��4��ǿ����Һ��ȼ�ϵ�ظ�����Ӧʽ����д���Է��IJ����У����ȣ�����Ԫ�ػ��ϼ۱仯���ȷ����������Ҫ��Ӧ��Ͳ����Σ����ݻ��ϼ���������ȷ��ʧȥ��������������������������ƽ�ⷴӦ���������ĵ��������ʹ���ҵ���غ㣻�����ˮʹ�����⡢��ԭ�Ӹ����غ㣻�����������״�����ȼ�ϵ�ظ�����ӦʽΪCH3OH+8OH����6e��==CO32��+ 6H2O��
���㣺���黯ѧ��Ӧԭ�����漰��ѧƽ��״̬�ı�־����ѧ��Ӧ���еķ�����������Է�Ӧ���ʺ�ƽ���ƶ���Ӱ��ͼ�����ʵ���Ũ�ȵļ��㡢��ѧƽ�ⳣ���ļ��㡢����ȼ�ϵ�ظ�����Ӧʽ����д�ȡ�

��Ԫ�صĻ����������������������Ź㷺��Ӧ�á�
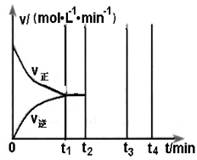
��1��400�棬1.01��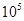 Pa�£��ݻ�Ϊ1��0L���ܱ������г���0.5molSO2, (g)��0.3 molO2 (g)��������Ӧ2SO2(g)��O2(g)
Pa�£��ݻ�Ϊ1��0L���ܱ������г���0.5molSO2, (g)��0.3 molO2 (g)��������Ӧ2SO2(g)��O2(g) 2SO3(g) ��H����198kJ/mol����Ӧ��n(SO3)��n(O2)��ʱ��仯�Ĺ�ϵ����ͼ��ʾ
2SO3(g) ��H����198kJ/mol����Ӧ��n(SO3)��n(O2)��ʱ��仯�Ĺ�ϵ����ͼ��ʾ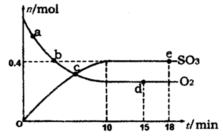 ����Ӧ��ƽ�ⳣ��K��_______��0��10 min����SO2��ʾ��ƽ����Ӧ����_________������ͼ����Ϣ���ж�������������ȷ����_____������ţ���
����Ӧ��ƽ�ⳣ��K��_______��0��10 min����SO2��ʾ��ƽ����Ӧ����_________������ͼ����Ϣ���ж�������������ȷ����_____������ţ���
| A��a��ʱ�̵�����Ӧ���ʱ�b��ʱ�̵Ĵ� |
| B��c��ʱ�̷�Ӧ�ﵽƽ��״̬ |
| C��d���e��ʱ�̵�c(O2)��ͬ |
| D����5 00�棬1.01��105Pa�£���Ӧ�ﵽƽ��ʱ��n( SO3) ��ͼ��e��ʱ�̵�ֵ�� |
��3����ͨ����ⷨʹ��2���е�����Һ������ѭ�����ã��缫��Ϊʯī�缫�����乤��ʾ��ͼ���£�
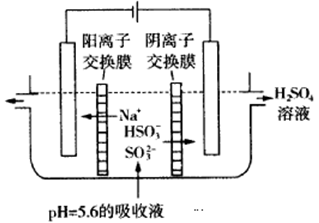
HSO3���������ҷ�Ӧ�ĵ缫��ӦʽΪ________________________�������ҵIJ���_________________��
̼���仯�����й㷺����;��
��1����ˮ����ͨ�����ȵ�̼���ɲ���ˮú������ӦΪ��
C(s)�� H2O(g)  CO(g) ��H2(g) ��H=" +131.3" kJ?mol-1�����Ϸ�Ӧ�ﵽƽ������������������£����´�ʩ���������H2O��ƽ��ת���ʵ��� ��(�����)
CO(g) ��H2(g) ��H=" +131.3" kJ?mol-1�����Ϸ�Ӧ�ﵽƽ������������������£����´�ʩ���������H2O��ƽ��ת���ʵ��� ��(�����)
| A�������¶ȡ� | B������̼������ | C��������� | D����CO���ռ���ȥCO |
 2CO��g�� ��H=+172.5kJ?mol-1
2CO��g�� ��H=+172.5kJ?mol-1��CO��g��+H2O��g��
 CO2��g��+H2��g�����ʱ��H=
CO2��g��+H2��g�����ʱ��H= ��3��CO��H2��һ�������¿ɷ�Ӧ���ɼ״���CO��g��+2H2��g��
 CH3OH��g�����״���һ��ȼ�ϣ������ü״����һ��ȼ�ϵ�أ���ϡ�������������Һ�����ʯī���缫���õ�ظ�����ӦʽΪ�� ��
CH3OH��g�����״���һ��ȼ�ϣ������ü״����һ��ȼ�ϵ�أ���ϡ�������������Һ�����ʯī���缫���õ�ظ�����ӦʽΪ�� �����øõ���ṩ�ĵ��ܵ��60mL NaCl��Һ������0.01molCH3OH��ȫ�ŵ磬NaCl�������ҵ�������Cl2ȫ����������ǰ�������Һ����ı仯�����������������Һ��pH=
��4����һ������CO(g)��H2O(g)�ֱ�ͨ�뵽���Ϊ2.0L�ĺ����ܱ������У��������·�Ӧ��
 CO(g)��H2O(g) CO2(g)��H2(g)���õ��������ݣ�
CO(g)��H2O(g) CO2(g)��H2(g)���õ��������ݣ�| �¶�/�� | ��ʼ��/mol | ƽ����/mol[ѧ�� | �ﵽƽ����x��ʱ��/min | ||
| H2O | CO | H2 | CO | ||
| 900 | 1.0 | 2.0 | 0.4 | 1.6 | 3.0 |
ͨ����������÷�Ӧ��ƽ�ⳣ��(���������λ��Ч����)����������������������
�ı䷴Ӧ��ijһ��������Ӧ���е�tminʱ����û��������CO2�����ʵ���Ϊ0.6 mol������200 mL 5 mol/L��NaOH��Һ������ȫ���գ���Ӧ�����ӷ���ʽΪ����һ�����ӷ���ʽ��ʾ����������������������������������������������
��5����ҵ�����ǰ�ˮú���еĻ�����徭���������õĽϴ�H2���ںϳɰ����ϳɰ���Ӧԭ��Ϊ��N2(g)+3H2(g)
 2NH3(g) ��H��-92.4kJ?mol-1��ʵ����ģ�⻯���������ֱ��ڲ�ͬʵ�������·�Ӧ��N2Ũ����ʱ��仯����ͼ��
2NH3(g) ��H��-92.4kJ?mol-1��ʵ����ģ�⻯���������ֱ��ڲ�ͬʵ�������·�Ӧ��N2Ũ����ʱ��仯����ͼ����ͬʵ�������·�Ӧ��N2Ũ����ʱ��仯����ͼ1��
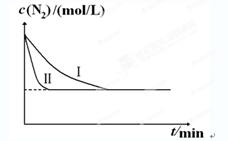

ͼ1 ͼ2
��ش��������⣺
����ʵ���Ƚϣ�ʵ���ı������Ϊ ��
��ʵ����ʵ�����¶�Ҫ�ߣ�����������ͬ��������ͼ2�л���ʵ����ʵ�����NH3Ũ����ʱ��仯��ʾ��ͼ��
������Ҫ���л��ϳ��м��壬�㷺Ӧ�����ܼ������ܼ������ϡ��ϼ���ӡˢ����֯�ȹ�ҵ������������ʵ���Һ�ҵ�Ʒ����������·�Ӧ��
CH3COOH��C2H5OH CH3COOC2H5��H2O
CH3COOC2H5��H2O
�����Ҫ��ش��������⣺
��1������������ת���ʣ��ɲ�ȡ�Ĵ�ʩ�У�__________��__________�ȡ�
��2��������ͼ��ʾ��װ�����Ʊ�������������������������ƫ�ͣ���ԭ�����Ϊ________��________�ȡ�
��3���˷�Ӧ��Ũ����Ϊ���������ܻ����__________��__________�����⡣
��4��Ŀǰ�Ը÷�Ӧ�Ĵ����������µ�̽����������������������Һ��������˷�Ӧ�Ĵ����������ظ�ʹ�á�ʵ���������±���ʾ��������Ҵ��Ե����ʵ�����ϣ���
| ͬһ��Ӧʱ�� | | ͬһ��Ӧ�¶� | ||||
| ��Ӧ�¶�/�� | ת���ʣ�%�� | ѡ���ԣ�%��* | | ��Ӧʱ��/h | ת���ʣ�%�� | ѡ���ԣ�%��* |
| 40 | 77.8 | 100 | | 2 | 80.2 | 100 |
| 60 | 92.3 | 100 | | 3 | 87.8 | 100 |
| 80 | 92.6 | 100 | | 4 | 92.3 | 100 |
| 120 | 94.5 | 98.7 | | 6 | 93.0 | 100 |
�ٸ��ݱ������ݣ�����________������ĸ��Ϊ�÷�Ӧ�����������
A��120 �棬4 h B��80 �棬2 h
C��60 �棬4 h D��40 �棬3 h
�ڵ���Ӧ�¶ȴﵽ120 ��ʱ����Ӧѡ���Խ��͵�ԭ�����Ϊ________��
��1����֪ ��ͬѧͨ���ⶨ�÷�Ӧ����ʱ��Һ����ǵ�ʱ�䣬�о���������Ի�ѧ��Ӧ���ʵ�Ӱ�졣���ʵ������(��ȡ��Һ�����Ϊl0mL)��
��ͬѧͨ���ⶨ�÷�Ӧ����ʱ��Һ����ǵ�ʱ�䣬�о���������Ի�ѧ��Ӧ���ʵ�Ӱ�졣���ʵ������(��ȡ��Һ�����Ϊl0mL)��
������������ʱ��̽���¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬Ӧѡ��ʵ��_______����ʵ���ţ�����ͬʱѡ��ʵ��١�ʵ��ڡ�ʵ��ۣ��ⶨ���Һ����ǵ�ʱ�ʣ���̽��_____�Ի�ѧ��Ӧ���ʵ�Ӱ�졣
��2��ijͬѧ�������ʵ������̽��Na2S2O3�Ļ�ѧ���ʡ�
�����ӷ���ʽ��ʾNa2S2O3��Һ���м��Ե�ԭ��_______,ʵ��������в���ʱpH��ֽ����ɫӦ�ýӽ� _______��
| A����ɫ | B������ɫ | C����ɫ | D����ɫ |
��ͬ�¶ȡ���ͬŨ�ȵ���Һ��pHֵ��С����
| A��NH4Cl | B��NH4HCO3 | C��NH4HSO4�� | D��(NH4)2 SO4 |
 E(g)
E(g)