题目内容
11.草酸是一种重要的化工原料,长用于有机合成,它属于二元弱酸,易溶于乙醇、水,微溶于乙醚,以甘蔗碎渣(主要成分为纤维素)为原料制取草酸的工业流程如下: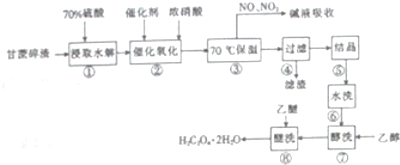
已知:
NO2+ZO+2NaOH═2NaNO2+H2O
2NO2+2NaOH═NaNO2+NaNO2+H2O
回答下列问题
(1)步骤①水解液中所含主要有机物为CH2OH-CHOH-CHOH-CHOH-CHOH-CHO(写结构式)浸取时要想提高水解速率除可减小甘蔗碎渣粒度外,还可采取的措施是适当提高温度浸取时硫酸浓度不宜过高,其原因是甘蔗碎渣会被炭化
(2)步驟②会生成草酸,硝酸的还原物为NO2和NO且n(NO2):n(NO)=3:1,则反应的离子方程式为C6H12O6+12H++12NO3-═3H2C2O4+9NO2↑+3NO↑+9H2O;生成的NO2及NO若被NaOH溶液完全吸收,则产物中的两种盐n(NaNO2):n(NaNO3)=3:1
(3)步驟③的主要目的是使葡萄糖充分氧化为草酸
(4)设计步骤⑦和⑧的目的分别是除去草酸表面的水分、除去乙醇使其快速干燥
(5)为了确定产品中H2C2O4.2H2O的纯度,称取10.5g草酸样品,配成250mL溶液,每次实验准确量取20.00mL,草酸溶液,加热适量的稀硫酸,用0.10mol.L-1的KMnO4标准溶液滴定,平行滴定三次,消耗KMnO4标准溶液的体积平均为26.00mL,则产品中H2C2O4.2H2O的质量分数为97.5%.
分析 甘蔗渣的主要成分为纤维素,70%硫酸做催化剂,浸取水解生成葡萄糖,结构简式为:CH2OH-CHOH-CHOH-CHOH-CHOH-CHO,加入稀硝酸,硝酸的还原物为NO2和NO,反应为:C6H12O6+12HNO3═3H2C2O4+9NO2↑+3NO↑+9H2O,生成的NO2及NO若被NaOH溶液完全吸收,NO+NO2+2NaOH═2NaNO2+H2O;2NO2+2NaOH═NaNO2+NaNO3+H2O,溶液中保持70℃,使葡萄糖充分氧化为草酸,过滤,滤液进行结晶得到草酸晶体,经过水洗、酸洗、乙醇、乙醚作用,得到H2C2O4.2H2O.
(1)甘蔗碎渣,其主要成分为纤维素,步骤①纤维素水解生成葡萄糖,水解为吸热反应,浸取时要想提高水解速率除可减小甘蔗碎渣粒度外,还可采取升高温度的措施,浓硫酸具有脱水性,浸取时硫酸浓度过高,蔗碎渣会被炭化;
(2)步驟②甘蔗渣水解生成的葡萄糖在70%的硫酸为催化剂的作用下,被硝酸氧化为草酸,同时生成NO2和NO,根据原子守恒、得失电子守恒书写方程式;生成的NO2及NO若被NaOH溶液完全吸收,根据反应:NO+NO2+2NaOH═2NaNO2+H2O;2NO2+2NaOH═NaNO2+NaNO3+H2O计算产物中的两种盐的物质的量之比;
(3)步驟③溶液中保持70℃,使葡萄糖充分氧化为草酸;
(4)乙醇易挥发,设计步骤⑦的目的是,除去草酸表面的水分,草酸微溶于乙醚,设计步骤⑧的目的是除去乙醇使其快速干燥;
(5)酸性高锰酸钾溶液具有强氧化性,能氧化草酸根离子生成二氧化碳,同时自身被还原生成二价锰离子,根据氧化还原反应得失电子守恒配平反应方程式,得关系式2KMnO4~5H2C2O4计算,注意溶液体积变化.
解答 解:(1)甘蔗碎渣,其主要成分为纤维素,纤维素属于多糖,水解生成葡萄糖,结构简式为CH2OH-CHOH-CHOH-CHOH-CHOH-CHO,浸取时,减小甘蔗碎渣粒度为增大接触面积,可提高水解速率,水解为吸热反应,采取升高温度的措施,也可提高水解速率,浓硫酸具有脱水性,浸取时硫酸浓度过高,蔗碎渣会被炭化,
故答案为:CH2OH-CHOH-CHOH-CHOH-CHOH-CHO;适当提高温度;甘蔗碎渣会被炭化;
(2)步驟②甘蔗渣水解生成的葡萄糖在70%的硫酸为催化剂的作用下,被硝酸氧化为草酸,同时生成NO2和NO,且n(NO2):n(NO)=3:1,则得到电子为3×1+1×3=6,葡萄糖中碳原子化合价为:0价,H2C2O4中碳原子化合价为+3价,需2个碳原子,即C6H12O6前系数为$\frac{1}{3}$,硝酸前系数为4,根据原子守恒,所以反应方程式为:C6H12O6+12HNO3═3H2C2O4+9NO2↑+3NO↑+9H2O,离子反应为:C6H12O6+12H++12NO3-═3H2C2O4+9NO2↑+3NO↑+9H2O,生成的NO2及NO若被NaOH溶液完全吸收,发生反应:NO+NO2+2NaOH═2NaNO2+H2O;2NO2+2NaOH═NaNO2+NaNO3+H2O,且n(NO2):n(NO)=3:1,所以产物中的两种盐n(NaNO2):n(NaNO3)=3:1,
故答案为:C6H12O6+12H++12NO3-═3H2C2O4+9NO2↑+3NO↑+9H2O;3:1;
(3)步驟③发生C6H12O6+12HNO3═3H2C2O4+9NO2↑+3NO↑+9H2O,生成NO2及NO,保持70℃,使葡萄糖充分氧化为草酸,
故答案为:使葡萄糖充分氧化为草酸;
(4)乙醇和水能以任意比互溶,乙醇易挥发,设计步骤⑦的目的是,除去草酸表面的水分,草酸微溶于乙醚,设计步骤⑧的目的是除去乙醇使其快速干燥,
故答案为:除去草酸表面的水分;除去乙醇使其快速干燥;
(5)酸性高锰酸钾溶液具有强氧化性,能氧化草酸根离子生成二氧化碳,同时自身被还原生成二价锰离子,离子反应为5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O,
由关系式 2KMnO4 ~5H2C2O4可知
2 5
0.1000mol•L-1×0.0260L n
解得:n=0.0065mol
100mL草酸溶液中草酸物质的量0.0065mol×$\frac{250}{20}$=0.08125mol
草酸晶体的质量分数=$\frac{0.08125mol×126g/mol}{10.50g}$×100%=97.5%;
故答案为:97.5%.
点评 本题考查氧化还原滴定原理与应用、探究影响速率的因素,题目难度中等,理解实验原理是解题的关键,是对知识的综合运用,需要学生具备扎实的基础知识与运用知识分析问题、解决问题的能力.

 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案①FeCl2 ②FeCl3 ③Fe(OH)3 ④HCl.
| A. | 只有①②③ | B. | 只有②③ | C. | 只有①③④ | D. | 全部 |
| A. | 质量为8.4g | B. | 物质的量为2 mol | ||
| C. | 体积为4.48 L | D. | 原子数目为0.56NA |
