题目内容
12.同温同压下,1体积气体A2与3体积气体B2恰好完全反应生成2体积的气体X,则X的化学式可表示为AB3,反应的化学方程式可表示为A2+3B2=2AB3.分析 同温同压下,气体摩尔体积相等,同一方程式中参加反应的气体体积之比等于其计量数之比,再结合原子守恒判断生成物化学式.
解答 解:同温同压下,气体摩尔体积相等,同一方程式中参加反应的气体体积之比等于其计量数之比,
则1体积气体A2与3体积气体B2恰好完全反应生成2体积的气体X,
所以该反应方程式为A2+3B2=2X,化学反应遵循各元素原子守恒,根据原子守恒C的化学式为AB3,则反应的化学方程式可表示为A2+3B2=2AB3;
故答案为:AB3;A2+3B2=2AB3.
点评 本题考查阿伏伽德罗定律及其推论,利用相同条件下气体体积与其反应计量数的关系即可解答,同时考查学生灵活运用知识能力,注意气体摩尔体积的适用范围及适用条件,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.已知物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等有关.下列各组物质:①Cu与HNO3溶液②Al与NaOH溶液③Zn与H2SO4溶液④Mg与HCl溶液.由于浓度不同而能发生不同氧化还原反应的是( )
| A. | ③④ | B. | ①③ | C. | ①② | D. | ①③④ |
4.下列叙述一定正确的是( )
| A. | Na2CO3溶液加水稀释后,恢复至原温度,pH和KW均减小 | |
| B. | 常温下,pH=2的一元酸和pH=12的一元强碱等体积混合:C(OH-)=C(H+) | |
| C. | 0.1mol•L-1NaOH溶液分别中和pH、体积均相同的醋酸和盐酸,所消耗Na0H溶液的体积前者小于后者 | |
| D. | 0.1mol•L-1CH3COONa溶液和0.1mol•L-1CH3COOH溶液混合后溶液pH<7:c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) |
1.下列离子方程式中书写不正确的是( )
| A. | 大理石与盐酸反应:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| B. | 少量金属钠放入冷水中:Na+2H2O=Na++2OH-+H2↑ | |
| C. | 二氧化硅与苛性钠溶液反应:SiO2+2OH-=SiO${\;}_{3}^{2-}$+H2O | |
| D. | 澄清石灰水通入过量CO2的总反应:CO2+OH-=HCO${\;}_{3}^{-}$ |
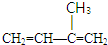 或
或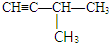 .
.