题目内容
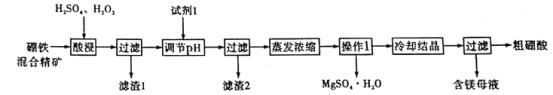
【题目】硫酸铜溶液可用于浸取硫铁矿中的铁,浸取时发生复杂的氧化还原反应,反应体系中除![]() 和
和![]() 外,还有
外,还有![]() 、
、![]() 、
、![]() 和
和![]() ,下列对该反应的分析不正确的是( )
,下列对该反应的分析不正确的是( )
A.氧化剂为![]() 和
和![]()
B.反应后溶液的pH降低
C.每转移2 mol电子消耗3 mol ![]()
D.被氧化的![]() 只占总量的30%
只占总量的30%
【答案】C
【解析】
由题干所给条件,可知反应物中应有![]() 和
和![]() ,生成物中应有
,生成物中应有![]() 和
和![]() ,再根据S原子守恒可知生成物还应该有
,再根据S原子守恒可知生成物还应该有![]() ,这样可写出反应方程式为:
,这样可写出反应方程式为:
![]() 。
。
A.![]() 中铜元素由正二价降低为正一价,为氧化剂;
中铜元素由正二价降低为正一价,为氧化剂;![]() 中的硫元素部分由负一价降低为二价,部分升高为正六价,即做氧化剂又做还原剂,所以氧化剂为
中的硫元素部分由负一价降低为二价,部分升高为正六价,即做氧化剂又做还原剂,所以氧化剂为![]() 和
和![]() ,不选A项;
,不选A项;
B.反应![]() 被消耗且有
被消耗且有![]() 生成,所以反应后溶液的pH降低,不选B项;
生成,所以反应后溶液的pH降低,不选B项;
C.由反应方程式![]() ,可知每转移21mol电子消耗14mol
,可知每转移21mol电子消耗14mol![]() ,即每转移3mol电子消耗2mol
,即每转移3mol电子消耗2mol![]() ,故选择C项;
,故选择C项;
D.由反应方程式![]() ,可知被还原的
,可知被还原的![]() 占:
占:![]() ;被氧化的
;被氧化的![]() 占:
占:![]() ,不选D项。
,不选D项。
答案选C。

练习册系列答案
相关题目