��Ŀ����
����Ŀ�����Ĺ̶�һֱ�ǿ�ѧ���о�����Ҫ���⣬�ϳɰ������˹��̵��Ƚϳ���ļ�������ԭ��ΪN2 (g)+3H2 (g)![]() 2NH3(g)
2NH3(g)
(1)��֪ÿ�ƻ�1mol�йػ�ѧ����Ҫ���������±���
H-H | N-H | N-N | N��N |
435.9KJ | 390.8KJ | 192.8KJ | 945.8KJ |
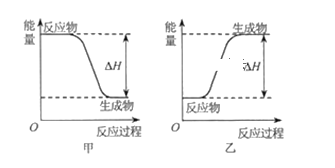
(1)��Ӧ���������_________(����>���� ��<��)�������������
(2)��һ���¶��¡���2L�ܱ������м���2 molN2��6 mol H2�����ʵ��Ĵ��������£�������Ӧ N2 (g)+3H2 (g)![]() 2NH3(g)��10min��ﵽƽ�⣬��ʱʣ��4.5mol H2��
2NH3(g)��10min��ﵽƽ�⣬��ʱʣ��4.5mol H2��
������������˵���˷�Ӧ�ﵽƽ��״̬����________________________��
a����������ѹǿ���� b��v(H2)����v(H2)���� c��N2��H2��Ũ�����
d�� 2 mol NH3���ɵ�ͬʱ��3 moH��H������ e��NH3��Ũ�Ȳ��ٸı�
��0��10 min�ڵ�ƽ����Ӧ����v(H2) ��______mol/(Lmin)��10��ĩNH3��Ũ����______mol/L��N2 �ĵ����ʵ���________mol
��ij�¶�ʱ����һ��2L���ܱ�������X��Y��Z�����������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ���ݴ˻ش�
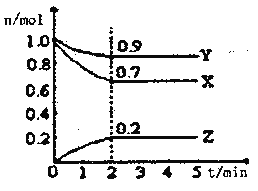
(1)�÷�Ӧ�Ļ�ѧ����ʽΪ_______________________
(2)�ӿ�ʼ��2min��Z��ƽ����Ӧ����Ϊ____________mol/(L��min)��
(3)�ı��������������Լӿ컯ѧ��Ӧ���ʵ���_________
A�������¶� B����С����X�����ʵ���
C����Сѹǿ D����������Z�����ʵ���.
E������ij�ִ��� F.��С�ݻ� G��ʹ��Ч�ʸ��ߵĴ���
(4)�÷�Ӧ����Ϊ���ȷ�Ӧ����������Ϊ��������(��������Ƚ���)����ƽ������ʱ�佫_________��
a���ӳ� b������ c������ d����ȷ��
���𰸡��� abe 0.075 0.5 1.5 3X+Y![]() 2Z 0.05 ADEFG b
2Z 0.05 ADEFG b
��������
��1�����������ݿ�֪��N2(g)+3H2(g)2NH3(g) ��H=��Ӧ������ܺ�-����������ܺ�=945.8kJ/mol+3��435.9kJ/mol-6��390.8kJ/mol=-91.3kJ/mol�����Ը÷�ӦΪ���ȷ�Ӧ������Ӧ���������������������������ʴ�Ϊ������
��2����a.�÷�Ӧ��Ӧǰ�������������ȣ��ʻ���������ѹǿ���ٷ����仯����Ϊ�ж��Ƿ�ﵽ��ѧƽ��״̬�����ݣ���a��ȷ��
b.v(H2)����v(H2)����˵�����淴Ӧ������ȣ�����Ϊ�ж��Ƿ�ﵽ��ѧƽ��״̬�����ݣ���b��ȷ��
c.ƽ��ʱN2��H2��Ũ��Ũ�Ȳ��ٷ����仯��������֮���Ũ�Ȳ�һ����Ȼ�����ij�ֹ�ϵ�������ж��Ƿ�ﵽ��ѧƽ��״̬����c����
d.��λʱ����2molNH3����Ϊ����Ӧ���ʣ�ͬʱ��3moH��H������ҲΪ����Ӧ���ʣ���Ϊ����Ӧ���ʣ������ж��Ƿ�ﵽ��ѧƽ��״̬����d����
e.NH3��Ũ�Ȳ��ٸı䣬˵����Ӧ�ﵽƽ��״̬����e��ȷ��
�ʴ�Ϊ��abe��
����2L�ܱ������м���2molN2��6 molH2�����ʵ��Ĵ��������£�������ӦN2(g)+3H2(g)![]() 2NH3(g)��10min��ﵽƽ�⣬��ʱʣ��4.5molH2����
2NH3(g)��10min��ﵽƽ�⣬��ʱʣ��4.5molH2����
N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
��ʼ����mol�� 2 6 0
ת������mol�� 0.5 1.5 1.0
ƽ������mol�� 1.5 4.5 1.0
0��10min�ڵ�ƽ����Ӧ����v(H2)= =0.075mol/(Lmin)��ƽ��ʱNH3��Ũ����
=0.075mol/(Lmin)��ƽ��ʱNH3��Ũ����![]() =0.5mol/L��N2�ĵ����ʵ���1.5mol���ʴ�Ϊ��0.075��0.5��1.5��
=0.5mol/L��N2�ĵ����ʵ���1.5mol���ʴ�Ϊ��0.075��0.5��1.5��
��1�������ߵı仯���ƿ��Կ������ӷ�Ӧ��ʼ���ﵽƽ�⣬X��Y�����ʵ������٣�ӦΪ��Ӧ�Z�����ʵ������ӣ�ӦΪ������ӷ�Ӧ��ʼ����2���ӷ�Ӧ����ƽ��״̬��X��Y���ĵ����ʵ����ֱ�Ϊ0.3mol��0.1mol��Z�����ɵ����ʵ���Ϊ0.2mol��������߱���Ϊ3��1��2�����ʵ����仯֮�ȵ��ڻ�ѧ������֮�ȣ���ѧ����ʽΪ3X+Y![]() 2Z���ʴ�Ϊ��3X+Y
2Z���ʴ�Ϊ��3X+Y![]() 2Z��
2Z��
��2���ӿ�ʼ��2min��Z��ƽ����Ӧ����Ϊv��Z��=![]() =
= =0.05mol/��Lmin�����ʴ�Ϊ��0.05��
=0.05mol/��Lmin�����ʴ�Ϊ��0.05��
��3��A.�����¶ȣ��ӿ췴Ӧ���ʣ���A��ȷ��
B.��С����X�����ʵ�������СX�Ķȣ���ѧ��Ӧ���ʽ��ͣ���B����
C.��Сѹǿ��������ѧ��Ӧ���ʣ���C����
D.��������Z�����ʵ���������Z��Ũ�ȣ���Ӧ���ʼӿ죬��D��ȷ��
E.����ij�ִ������ӿ췴Ӧ���ʣ���E��ȷ��
F.��С�ݻ�������Ӧ���Ũ�ȣ���Ӧ���ʼӿ죬��F��ȷ��
G.ʹ��Ч�ʸ��ߵĴ������ӿ췴Ӧ���ʣ���G��ȷ��
�ʴ�Ϊ��ADEFG��
��4������������Ϊ��������(��������Ƚ���)���÷�Ӧ������ӦΪ���ȷ�Ӧ�������൱�������¶ȣ���Ӧ���ʼӿ죬�����̵���ƽ������ʱ�䣬��ѡb���ʴ�Ϊ��b��

����Ŀ������ʵ���������������ý��۾���ȷ����( )
ѡ�� | ʵ������ | ʵ����� |
A | ��ʢ��5mL0.005mol/L FeCl3��Һ�м���5mL0.01mol/LKSCN��Һ���ټ�����������KCl���壬�۲����� | ֤����Һ����ƽ�⣺ FeCl3+3KSCNFe(SCN)3+3KCl |
B | ȡ��ֻ�Թܣ��ֱ����������Ũ�ȵ�˫��ˮ��Ȼ���Թ����м���0.01mol/LFeCl3��Һ2mL���Թ����м���0.01mol/LCuCl2��Һ2mL���Թ����������ݿ� | ����FeCl3ʱ��˫��ˮ�ֽⷴӦ�Ļ�ܽϴ� |
C | ����FeCl3��Һ���Ƿ���Fe2+ʱ������Һ��������KMnO4��Һ����Һ�Ϻ�ɫ��ȥ | ����֤����Һ�к���Fe2+ |
D | ȡ��ֻ�Թֱܷ����4mL0.01mol/LKMnO4������Һ��Ȼ����һֻ�Թ��м���0.01mol/L H2C2O4��Һ2mL������һֻ�Թ��м���0.01mol/L H2C2O4��Һ4mL����һֻ�Թ�����ɫʱ�䳤 | H2C2O4Ũ��Խ��Ӧ����Խ�� |
A.AB.BC.CD.D