题目内容
【题目】(1)写出N2的电子式_____。下列能实现人工固氮的是____。
A.闪电 B.在加压降温的条件下使空气中的氮气液化
C.根瘤 D.合成氨车间
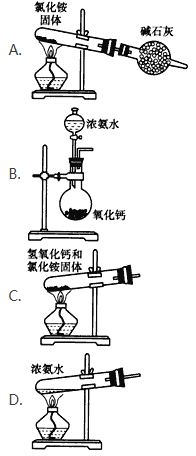
(2)实验室通常用加热消石灰与氯化铵固体的方法来制取氨气。写出该反应的化学方程式____。实验室制取氨气的方法有多种,下面的装置和选用的试剂中错误的是____。
(3)氨气可使湿润的红包石蕊试纸变蓝的原因(用化学用语表示)______。
(4)用乙装置吸收一段时间氨后,再通入空气,同时将加热的铜丝插入乙装置的锥形瓶内,锥形瓶中不可能生成的物质是:____。
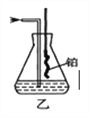
A. H2 B. NO2 C.HNO3 D. NH4N03
写出乙装置中氨催化氧化的化学方程式:______。
(5)已知3Cl2+2NH3→N2+6HCl,常温常压下,在一密闭容器中将15mLCl2和40mLNH3充分反应后,剩余气体的体积为_____mL。
(6)在标准状况下,1L水中可溶解700LNH3,所得溶液的密度为0.9g/cm3,则氨水的物质的量浓度为_____mol/L(保留一位小数)。
【答案】 ![]() D Ca(OH)2+2NH4Cl
D Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O AC NH3+ H2O
CaCl2+2NH3↑+2H2O AC NH3+ H2O![]() NH3· H2O
NH3· H2O![]() NH4++ OH— A 4NH3+5O2
NH4++ OH— A 4NH3+5O2![]() 4NO+6H2O 5 18.4
4NO+6H2O 5 18.4
【解析】(1)N2分子中含有三键,电子式为![]() 。游离态氮元素转化为化合态氮元素的过程是氮的固定,A.闪电是自然固氮,A错误;B.在加压降温的条件下使空气中的氮气液化是物理变化,B错误;C.根瘤菌固氮是自然固氮,C错误;D.合成氨车间属于人工固氮,D正确,答案选D。(2)实验室通常用加热消石灰与氯化铵固体的方法来制取氨气,该反应的化学方程式为Ca(OH)2+2NH4Cl
。游离态氮元素转化为化合态氮元素的过程是氮的固定,A.闪电是自然固氮,A错误;B.在加压降温的条件下使空气中的氮气液化是物理变化,B错误;C.根瘤菌固氮是自然固氮,C错误;D.合成氨车间属于人工固氮,D正确,答案选D。(2)实验室通常用加热消石灰与氯化铵固体的方法来制取氨气,该反应的化学方程式为Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O。A、氯化铵受热分解生成的氯化氢和氨气在试管口又转化为氯化铵,A错误;B、氧化钙溶于水生成氢氧化钙,反应放热,且氢氧根浓度增大,所以可以用浓氨水和生石灰反应制备氨气,B正确;C、试管口应该略低于试管底,C错误;D、直接加热浓氨水可以制备氨气,D正确,答案选AC。(3)氨气溶于水生成一水合氨,一水合氨电离出氢氧根,可使湿润的红包石蕊试纸变蓝,方程式为NH3+ H2O
CaCl2+2NH3↑+2H2O。A、氯化铵受热分解生成的氯化氢和氨气在试管口又转化为氯化铵,A错误;B、氧化钙溶于水生成氢氧化钙,反应放热,且氢氧根浓度增大,所以可以用浓氨水和生石灰反应制备氨气,B正确;C、试管口应该略低于试管底,C错误;D、直接加热浓氨水可以制备氨气,D正确,答案选AC。(3)氨气溶于水生成一水合氨,一水合氨电离出氢氧根,可使湿润的红包石蕊试纸变蓝,方程式为NH3+ H2O![]() NH3· H2O
NH3· H2O![]() NH4++ OH-。(4)氨气与氧气催化氧化生成了一氧化氮和水,一氧化氮能够与氧气生成二氧化氮,二氧化氮与水反应生成一氧化氮和硝酸,硝酸能够与氨气反应生成硝酸铵,所以不可能生成的是氢气,答案选A;氨气催化氧化的反应的方程式为4NH3+5O2
NH4++ OH-。(4)氨气与氧气催化氧化生成了一氧化氮和水,一氧化氮能够与氧气生成二氧化氮,二氧化氮与水反应生成一氧化氮和硝酸,硝酸能够与氨气反应生成硝酸铵,所以不可能生成的是氢气,答案选A;氨气催化氧化的反应的方程式为4NH3+5O2![]() 4NO+6H2O;(5)15ml Cl2和40ml NH3反应,根据反应方程式3Cl2+2NH3=N2+6HCl,15mL氯气反应消耗氨气10mL氨气,生成5mL氮气和30mL氯化氢;由于氨气与氯化氢反应生成氯化铵,剩余的氨气恰好与生成的氯化铵反应,因此最后剩余的气体是氮气,体积为5mL;(6)氨气的物质的量为:700L/22.4L/mol=31.25mol,溶液的质量为:1000g+17×31.25g=1531.25g,氨水溶液的体积为:1531.25g÷0.90.9g/cm3≈1700mL=1.70L,所以氨水的浓度为:31.25mol÷1.7L≈18.4mol/L。
4NO+6H2O;(5)15ml Cl2和40ml NH3反应,根据反应方程式3Cl2+2NH3=N2+6HCl,15mL氯气反应消耗氨气10mL氨气,生成5mL氮气和30mL氯化氢;由于氨气与氯化氢反应生成氯化铵,剩余的氨气恰好与生成的氯化铵反应,因此最后剩余的气体是氮气,体积为5mL;(6)氨气的物质的量为:700L/22.4L/mol=31.25mol,溶液的质量为:1000g+17×31.25g=1531.25g,氨水溶液的体积为:1531.25g÷0.90.9g/cm3≈1700mL=1.70L,所以氨水的浓度为:31.25mol÷1.7L≈18.4mol/L。