题目内容
【题目】请回答下列问题:
Ⅰ.工业生产纯碱的工艺流程示意图如图:
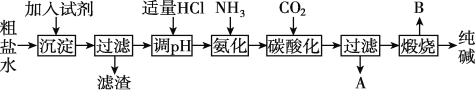
(1)为除去粗盐水中的Mg2+、Ca2+、SO42-等杂质离子,加入试剂顺序合理的是____。
A.碳酸钠、氢氧化钠、氯化钡
B.碳酸钠、氯化钡、氢氧化钠
C.氢氧化钠、碳酸钠、氯化钡
D.氯化钡、氢氧化钠、碳酸钠
(2)工业生产纯碱工艺流程中,碳酸化时产生的现象是____;碳酸化时没有析出碳酸钠晶体,其原因是____。
(3)碳酸化后过滤,滤液A最主要的成分是____(填写化学式),检验这一成分的阴离子的具体方法是____。
(4)煅烧制取Na2CO3在____(填字母序号)中进行。
a.瓷坩埚 b.蒸发皿 c.铁坩埚 d.氧化铝坩埚
Ⅱ.纯碱在生产生活中有广泛的用途。
(5)工业上,可用纯碱代替烧碱生产某些化工产品。如用饱和纯碱溶液与氯气反应可制得有效成分为次氯酸钠的消毒液,其反应的离子方程式为____。
【答案】D 有晶体析出(或出现浑浊) 碳酸钠溶解度比碳酸氢钠大 NH4Cl 取样,加硝酸酸化,加硝酸银溶液,有白色沉淀生成,则该阴离子是氯离子 c 2CO32-+Cl2+H2O=2HCO3-+Cl-+ClO-
【解析】
粗盐水中的Mg2+、Ca2+、SO42-等杂质离子,先加BaCl2(NaOH),再加NaOH (BaCl2),最后加入Na2CO3,除去Mg2+、Ca2+、SO42-;加入适量的HCl,除去OH-和CO32-;氨化、碳酸化,过滤滤液A为NH4Cl,煅烧制取Na2CO3。
(1)在粗盐提纯过程中,所加除杂试剂的顺序通常为先加BaCl2,再加NaOH,最后加入Na2CO3。加NaOH的顺序可以放在BaCl2的前面也可以放在Na2CO3的后面,但Na2CO3的加入顺序必须放在BaCl2的后面,因过量的BaCl2需用Na2CO3除去,选D,故答案为:D;
(2)纯碱生产过程中碳酸化时,会看到溶液中有晶体析出,没有析出Na2CO3晶体是由于碳酸钠的溶解度大于碳酸氢钠的,故答案为:有晶体析出(或出现浑浊);碳酸钠溶解度比碳酸氢钠大;
(3)根据操作过程,碳酸化后的溶液中主要溶质是NH4Cl;检验其中的氯离子时,要先取样,滴加稀硝酸酸化,再加硝酸银溶液,有白色沉淀生成,可知阴离子是氯离子,故答案为:NH4Cl;取样,加硝酸酸化,加硝酸银溶液,有白色沉淀生成,则该阴离子是氯离子;
(4)Na2CO3显碱性,瓷坩埚、蒸发皿为SiO2,与Na2CO3反应,高温条件下氧化铝也与Na2CO3反应,所以选c,故答案为:c。
(5)氯气和氢氧化钠反应时生成氯化钠、次氯酸钠和水:Cl2+2NaOH=NaCl+NaClO+H2O;纯碱溶液呈碱性,Na2CO3+H2O![]() NaHCO3+NaOH,则饱和纯碱溶液与Cl2反应的化学方程式为:2Na2CO3+Cl2+H2O=NaCl+NaClO+2NaHCO3,其离子反应方程式为:2CO32-+Cl2+H2O=2HCO3-+Cl-+ClO-;故答案为:2CO32-+Cl2+H2O=2HCO3-+Cl-+ClO-。
NaHCO3+NaOH,则饱和纯碱溶液与Cl2反应的化学方程式为:2Na2CO3+Cl2+H2O=NaCl+NaClO+2NaHCO3,其离子反应方程式为:2CO32-+Cl2+H2O=2HCO3-+Cl-+ClO-;故答案为:2CO32-+Cl2+H2O=2HCO3-+Cl-+ClO-。