题目内容
【题目】用活性炭还原处理氮氧化物,有关反应为C(s)+2NO(g) ![]() N2(g)+CO2(g)。
N2(g)+CO2(g)。
(1)写出上述反应的平衡常数表达式_______________。
(2)在2L恒容密闭器中加入足量C与NO发生反应,所得数据如表,回答下列问题。
实验编号 | 温度/℃ | 起始时NO的物质的量/mol | 平衡时N2的物质的量/mol |
1 | 700 | 0.40 | 0.09 |
2 | 800 | 0.24 | 0.08 |
①结合表中数据,判断该反应的△H____0(填“>”或“<”),理由是_________。
②判断该反应达到平衡的依据是_______。
A.容器内气体密度恒定 B.容器内各气体浓度恒定
C.容器内压强恒定 D.2v正(NO)= v逆(N2)
(3)700℃时,若向2L体积恒定的密闭容器中充入一定量N2和CO2发生反应:N2(g)+CO2(g)![]() C(s)+2NO(g) ;其中N2、NO物质的量随时间变化的曲线如下图所示。请回答下列问题。
C(s)+2NO(g) ;其中N2、NO物质的量随时间变化的曲线如下图所示。请回答下列问题。
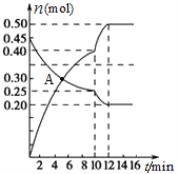
①0~10 min内的CO2平均反应速率v=____________。
②图中A点v(正)___v(逆)(填“>”、“<”或“=”)。
③第10 min时,外界改变的条件可能是_____________。
A.加催化剂 B.增大C的物质的量
C.减小CO2的物质的量 D.升温 E.降温
【答案】 ![]() > 计算700℃和800℃的平衡常数K1<K2,所以△H >0 AB 0.01 mol·L-1·min-1 > AD
> 计算700℃和800℃的平衡常数K1<K2,所以△H >0 AB 0.01 mol·L-1·min-1 > AD
【解析】K=![]()
(2)①根据表格数据,列出实验1(700℃)的三段式:
C(s)+2NO(g)N2(g)+CO2(g)
起始物质的量/mol 0.4 0 0
变化物质的量/mol 0.18 0.09 0.09
平衡物质的量/mol 0.22 0.09 0.09
K1=![]() =
=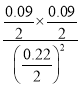 =
=![]() ,
,
据表格数据,列出实验2(℃)的三段式:
C(s)+2NO(g)N2(g)+CO2(g)
起始物质的量/mol 0.24 0 0
变化物质的量/mol 0.16 0.08 0.08
平衡物质的量/mol 0.08 0.08 0.08
K2=![]() =
=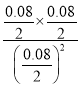 =1>K1;
=1>K1;
温度升高,K增大,则正反应为吸热反应,△H>0。
故答案为:>;700℃和800℃的平衡常数K1<K2,所以△H >0。
②A、该反应气体的总质量是个变量,容器体积不变,所以密度是一个变量,当容器内气体密度恒定时,则反应达到平衡状态,故A正确;B、各组分的浓度不再改变能说明反应达到平衡状态,故B正确;C、该反应前后气体分子的数目相同,则气体的总物质的量一直不变,根据pV=nRT,恒温恒容条件下,压强一直不变,所以容器内压强恒定不能说明反应达到平衡状态,故C错误;D、2v正(NO)= v逆(N2)错误,此时正反应速率和逆反应速率不相等,应是v正(NO)= 2v逆(N2)时反应达到平衡状态故D错误。故选AB。
故答案为:AB。
③①随着反应进行,n(N2)逐渐减小,n(NO)逐渐增大,10min内,△n(N2)=0.2mol,物质的量变化之比等于计量系数之比,则△n(CO2)=0.2mol,所以v(CO2)= ![]() =0.01 mol·L-1·min-1;
=0.01 mol·L-1·min-1;
②根据图像可知A点反应向正反应方向进行,则v(正)>v(逆),故答案为:>;
③第10min时,N2、NO物质的量没有发生突变,N2的物质的量逐渐减小,速率比10min前大;NO物质的量逐渐增大,速率比10min前大。A、加催化剂,不会引起物质的量的突变,只会增大反应速率,故A正确;B、增大碳固体的物质的量,对反应速率没有影响,故B错误;C、减小CO2的物质的量,反应速率减小,故C错误;D、升温,反应速率增大,故D正确;E、降温,反应速率减小,故E错误。故选AD。

【题目】叠氮酸钠(NaN3)是一种应用广泛的无色无味、可溶于水的晶体。已知:
物质 | CH3OH | N2H4 | NaN3 |
沸点/℃ | 64.7 | 113.5 | 300 |
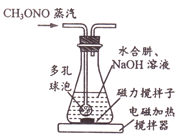
(1)制备NaN3:
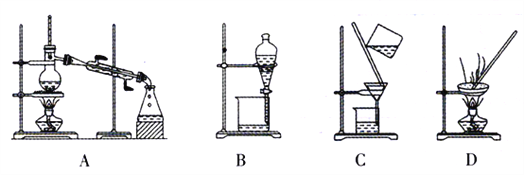
30℃时,水合肼(N2H4H2O)与亚硝酸甲酯(CH3ONO)、NaOH反应,装置如右图所示。反应后锥形瓶中混合物经“操作X”可回收CH3OH,母液降温结晶,过滤得NaN3粗品,重结晶得到NaN3产品。
①装置中的多孔球泡的作用是______。
②写出生成NaN3的化学方程式:_________________。
③“操作X”的名称为________________。
(2)测定NaN3产品纯度: ①称取NaN3产品5.0000g,用适量稀硫酸溶解后配成100.00mL溶液A;②取25.00mL溶液A,加入20.00mL0.2000mol/LKMnO4溶液,得紫红色溶液B;
③向溶液B加入足量KI溶液消耗过量的KMnO4溶液,然后以淀粉作指示剂,用0.1000mol/LNa2S2O3标准溶液滴定产生的I2,消耗Na2S2O3溶液30.00mL。测定过程中物质的转化关系如下:
10NaN3+2KMnO4+8H2SO4=2MnSO4+K2SO4+5Na2SO4+8H2O+15N2↑
I- ![]() I2
I2 ![]() S4O62-
S4O62-
计算NaN3产品的纯度(写出计算过程)。_____________________