题目内容
【题目】下列叙述中正确的是( )
A. 原电池中的负极失电子,发生还原反应
B. 原电池中发生氧化反应的电极是负极
C. 原电池中的电极一定要由两种不同的金属组成
D. 原电池中较活泼的金属做正极
【答案】B
【解析】
A. 原电池中的负极失去电子,发生氧化反应,A项错误;
B.原电池中负极发生氧化反应,正极发生还原反应,所以发生氧化反应的电极是负极,B项正确;
C.原电池中的电极不一定要由两种不同的金属组成,如燃料电池的正、负极都可以使用金属铂(或都用石墨),其中金属铂不仅作电极,而且还起催化转化作用。C项错误;
D.一般来说,两种活泼性不同的金属作原电池两极时,较活泼的金属做负极,D项错误;答案选B。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】用活性炭还原处理氮氧化物,有关反应为C(s)+2NO(g) ![]() N2(g)+CO2(g)。
N2(g)+CO2(g)。
(1)写出上述反应的平衡常数表达式_______________。
(2)在2L恒容密闭器中加入足量C与NO发生反应,所得数据如表,回答下列问题。
实验编号 | 温度/℃ | 起始时NO的物质的量/mol | 平衡时N2的物质的量/mol |
1 | 700 | 0.40 | 0.09 |
2 | 800 | 0.24 | 0.08 |
①结合表中数据,判断该反应的△H____0(填“>”或“<”),理由是_________。
②判断该反应达到平衡的依据是_______。
A.容器内气体密度恒定 B.容器内各气体浓度恒定
C.容器内压强恒定 D.2v正(NO)= v逆(N2)
(3)700℃时,若向2L体积恒定的密闭容器中充入一定量N2和CO2发生反应:N2(g)+CO2(g)![]() C(s)+2NO(g) ;其中N2、NO物质的量随时间变化的曲线如下图所示。请回答下列问题。
C(s)+2NO(g) ;其中N2、NO物质的量随时间变化的曲线如下图所示。请回答下列问题。
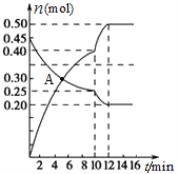
①0~10 min内的CO2平均反应速率v=____________。
②图中A点v(正)___v(逆)(填“>”、“<”或“=”)。
③第10 min时,外界改变的条件可能是_____________。
A.加催化剂 B.增大C的物质的量
C.减小CO2的物质的量 D.升温 E.降温