题目内容
16.已知苯、溴和溴苯的物理性质如下表所示| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |

填写下列空白:
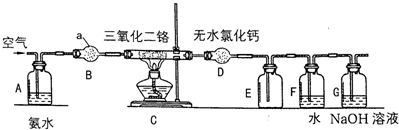
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应.写出A中所发生反应的化学方程式(有机物写结构简式):
 .
.(2)试管C中苯的作用是除去溴化氢中混有的溴蒸汽;反应开始后,观察D试管,看到的现象为石蕊试液变红,并在导管中有白雾产生
(3)在上述整套装置中,具有防倒吸作用的仪器有DEF(填字母).
(4)反应完毕后,将a瓶中的液体取出,经过分液 (填分离操作的名称)可获得获得粗溴苯,向粗溴苯中加入无水CaCl2,其目的是干燥
(5)经以上分离操作后,要进一步提纯粗溴苯,下列操作中必须的是C(填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取.
分析 本题是对苯和液溴反应原理的探究,对课本实验进行了改进,涉及反应后的混合液的分离提纯和对实验过程中溴化氢的检验,反应混合物静置后分层可分液分离,得到的粗溴苯中仍混有的苯因混溶可通过蒸馏进一步分离,因溴的挥发,检验溴化氢时要先排除溴的干扰,并借助硝酸银溶液里有浅黄色沉淀来证明溴化氢的存在,同时还要注意尾气处理,本题综合性较强.
(1)根据苯和液溴发生取代反应生成溴苯和溴化氢解答;
(2)溴苯中的溴易挥发,非极性分子的溶质易溶于非极性分子的溶剂,据此分析苯的作用;该反应中有溴化氢生成,溴化氢溶于水得到氢溴酸,氢溴酸能使石蕊试液变红色;
(3)因溴化氢极易溶解于水,导气管不插入溶液中、倒置漏斗或球形干燥管能防止溶液倒吸;
(4)反应后的混合液含有有机物和无机混合液,因相互不溶,静置后会出现分层现象,可选择分液漏斗进行分液操作,无水CaCl2有吸水性,加入到粗产品中可除去混有的少量水份;
(5)获得的粗溴苯中仍混合相互混的苯和少量溴,可根据各组分的沸点差异进行分离.
解答 解:(1)在催化剂的作用下,苯环上的氢原子溴原子所取代,生成溴苯,同时有溴化氢生成,反应为,
故答案为: ;
;
(2)溴苯中的溴易挥发,溴和苯都是非极性分子,根据相似相溶原理知,溴易溶于苯,所以苯的作用是吸收溴蒸汽;该反应中有溴化氢生成,溴化氢溶于水得到氢溴酸,氢溴酸是酸性物质,能使石蕊试液变红色;所以观察D看到的现象是D管中石蕊试液变红;
故答案为:除去HBr中混有的溴蒸气;石蕊试液变红;
(3)当两端压力发生压力变化时,液体会产生倒吸现象,DE装置中导气管不插入溶液中可以防止倒吸,倒置的漏斗下口很大,液体上升很小的高度就有很大的体积,上升的液体的本身的压力即可低偿压力的不均衡.因此由于上部还有空气隔离,液体不会倒吸入上端的细管道,所以具有防倒吸作用的仪器有DEF,故答案为:DEF;
(4)反应后的混合液静置后会出现分层现象,可选择分液漏斗进行分液操作,得到的粗溴苯中仍有少量水溶液,可加入无水CaCl2利用其有吸水性,达到吸水干燥的目的,故答案为:分液;干燥;
(5)粗溴苯中仍含有苯、溴,由于三者互溶在一起,而且它们的沸点不同,所以可采用蒸馏的方法来分离,故答案为:蒸馏.
点评 本题考查了苯的取代反应实验,考查的知识点有反应方程式的书写、产物的判断、蒸汽的成分及性质,综合性较强,难度较大,注意苯能和液溴发生取代反应,和溴水不反应.

 名校课堂系列答案
名校课堂系列答案| A. | 1:3 | B. | 1:2 | C. | 2:3 | D. | 3:2 |
(1)常温常压下,二氧化碳加氢可选择性生成二甲醚或一氧化碳:
①CO2(g)+3H2(g)?CH3OH(l)+H2O(l)△H=-55.7kJ/mol
②2CH3OH(l)?CH3OCH3(g)+H2O (l)△H=-23.4kJ/mol
则CO2(g)加氢转化为CH3OCH3(g)和H2O (l)的热化学方程式是:2CO2(g)+6H2(g)=CH3OCH3(g)+3 H2O(l)△H=-134.8kJ/mol.
(2)CO2合成尿素的反应为:CO2(g)+2NH3(g)?CO(NH2)2(l)+H2O (g)△H<0.该反应的平衡常数表达式为$\frac{c({H}_{2}O)}{c(C{O}_{2})×{c}^{2}(N{H}_{3})}$.
(3)实验室模拟用CO和H2反应来制甲醇:CO(g)+2H2(g)?CH3OH(g)△H<0.在250℃下,将一定量的CO和H2投入10L的密闭容器中,各物质的物质的量浓度(mol•L-1)变化如下表所示:(前6min没有改变条件)
| 2min | 4min | 6min | 8min | … | |
| CO | 0.07 | 0.06 | 0.06 | 0.05 | … |
| H2 | x | 0.12 | 0.12 | 0.2 | … |
| CH3OH | 0.03 | 0.04 | 0.04 | 0.05 | … |
②250℃时该反应的平衡常数K值为:$\frac{0.04}{0.06×0.1{2}^{2}}$mol-2.L2(不必化简).
③若6min~8min只改变了某一条件,所改变的条件是加入1mol氢气.
④第8min时,该反应是不是达到平衡状态不是.(填“是”或“不是”)
⑤该合成反应的温度一般控制在240~270℃,选择此温度的原因是:Ⅰ.此温度下的催化剂活性高;Ⅱ.温度低,反应速率慢,单位时间内的产量低,而正反应为放热反应,温度过高,转化率降低.
| 甲 | 乙 | 丙 | 丁 | ||
| 起始物质的量 | n(SO2)/mol | 0.40 | 0 | 0.80 | 0.02 |
| n(O2)/mol | 0.24 | 0 | 0.48 | 0.04 | |
| n(SO3)/mol | 0 | 0.40 | 0 | 0.40 | |
| 含硫反应物的平衡转化率% | 80 | a1 | a2 | a3 | |
| A. | 该温度下,平衡常数的值为400 | B. | 平衡时,丙中c(SO3)是甲中的2倍 | ||
| C. | 平衡时,a3>a1 | D. | 乙中SO3的平衡转化率为a1=20% |
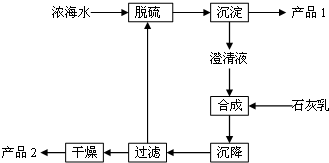 将海水淡化后,从剩余的浓海水中通过一系列工艺流程可以生产其他产品.
将海水淡化后,从剩余的浓海水中通过一系列工艺流程可以生产其他产品.(1)Cl2可以氧化浓海水中的Br-,用空气吹出Br2,并用纯碱吸收.纯碱吸收溴的主要反应是Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(化学方程式未配平),则吸收1mol Br2时,该反应转移的电子为$\frac{5}{3}$mol.
(2)精制浓海水可以得到纯净的饱和食盐水,向其中加入碳酸氢铵可制备碳酸氢钠.
①NaCl的电子式是
 .
.②上述制备碳酸氢钠的化学方程式是NaCl+NH4HCO3═NaHCO3↓+NH4Cl.
③为测定制得的碳酸氢钠的纯度,可称量a g碳酸氢钠样品(含少量NaCl)溶于足量盐酸,蒸干溶液后灼烧,剩余固体质量为b g.样品碳酸氢钠的质量分数是$\frac{84(a-b)}{25.5a}$×100%(用含a、b的代数式表示).
(3)海水提取镁的一段工艺流程如图:
浓海水中的有关成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g•L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
②产品2的化学式为Mg(OH)2;1L浓海水最多可得到产品2的质量为69.6 g.
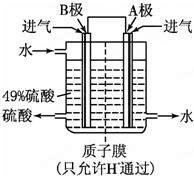 硫酸厂用煅烧黄铁矿(FeS2)来制取硫酸,实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制备绿矾.
硫酸厂用煅烧黄铁矿(FeS2)来制取硫酸,实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制备绿矾.