题目内容
8.有下列实验事实:①0.1mol•L-1 的NaA溶液呈碱性;
②将0.1mol•L-1 HA溶液加水稀释100倍,pH变化小于2;
③HA溶液和Na2CO3溶液反应能产生CO2;
④同体积同浓度的盐酸和HA溶液分别与相同的锌粒反应,盐酸反应快.
(1)上述事实中能证明某酸HA为弱电解质的是①②④.
(2)为证明HA是弱酸,甲同学提出方案:
用pH试纸测出0.1mol•L-1的HA溶液的pH,即可证明HA是弱酸.
甲同学方案中,说明HA是弱电解质的理由是:测得溶液的pH>1(选填>、<、=).
(3)乙同学又提出一新方案:
1.分别配制pH=l的HA溶液和盐酸各10mL,均加水稀释为100mL;
2.分别取两种稀释液少许,同时加入相同的锌粒,观察现象即可证明HA是弱酸.
乙同学方案中,说明HA是弱电解质的现象是b(填序号)
a.反应中装HCl溶液的试管中放出H2的速率快;
b.反应中装HA溶液的试管中放出H2的速率快;
c.反应中两个试管中产生气体速率一样快.
(4)若HA、HB均为弱酸,请你设计实验方案,证明二者酸性的强弱方案一:取同浓度的NaA、NaB溶液分别测其pH的大小,若pH前者大于后者,则证明酸性HA小于HB;
方案二:取等体积、等浓度的HA、HB溶液,分别与足量的颗粒大小相同的锌粒反应,产生气泡较快者的酸性较强;
方案三:取相同体积、相同pH的HA、HB溶液,分别加水稀释相同的倍数后测定pH,pH变化大者酸性较强.
分析 (1弱电解质在水溶液里或熔融状态下部分电离,只要说明HA部分电离就能证明HA是弱电解质;
(2)弱电解质在水溶液中部分电离,一元弱酸部分电离导致氢离子浓度小于溶液酸浓度;
(3)等浓度的一元强酸和一元弱酸中,强酸中的氢离子浓度大于弱酸;
(4)酸的强弱可以根据相同浓度的钠盐溶液pH大小判断,可以根据相同浓度、相同体积的酸溶液与相同的金属反应置换出氢气快慢判断,可以根据相同体积相同pH的溶液稀释相同倍数pH变化判断.
解答 解:(1)①0.1mol•L-1 的NaA溶液呈碱性,说明NaA是强碱弱酸盐,则HA是弱酸,故正确;
②将0.1mol•L-1 HA溶液加水稀释100倍,pH变化小于2,说明HA中存在电离平衡,则说明HA是弱电解质,故正确;
③HA溶液和Na2CO3溶液反应能产生CO2,说明HA酸性大于碳酸,碳酸是弱酸,不能说明HA是强酸还是弱酸,故错误;
④同体积同浓度的盐酸和HA溶液分别与相同的锌粒反应,盐酸反应快,说明HA中氢离子浓度小于盐酸,则HA部分电离,为弱电解质,故正确;
故答案为:①②④;
(2)配制0.1mol/L的HA酸溶液100mL,弱电解质的电离是可逆的,不能完全电离,测得溶液的H+的浓度<0.1mol•L-1,溶液的pH>1
故答案为:>;
(3)pH相等的HA和盐酸,随着反应进行,弱酸继续电离出氢离子而导致反应过程中弱酸氢离子浓度大于盐酸,所以弱酸反应速率更快,故选b,
(4)酸的强弱可以根据相同浓度的钠盐溶液pH大小判断,可以根据相同浓度、相同体积的酸溶液与相同的金属反应置换出氢气快慢判断,可以根据相同体积相同pH的溶液稀释相同倍数pH变化判断,其实验方案为:
方案一:取同浓度的NaA、NaB溶液分别测其pH的大小,若pH前者大于后者,则证明酸性HA小于HB;
方案二:取等体积、等浓度的HA、HB溶液,分别与足量的颗粒大小相同的锌粒反应,产生气泡较快者的酸性较强;
方案三:取相同体积、相同pH的HA、HB溶液,分别加水稀释相同的倍数后测定pH,pH变化大者酸性较强,
故答案为:方案一:取同浓度的NaA、NaB溶液分别测其pH的大小,若pH前者大于后者,则证明酸性HA小于HB;
方案二:取等体积、等浓度的HA、HB溶液,分别与足量的颗粒大小相同的锌粒反应,产生气泡较快者的酸性较强;
方案三:取相同体积、相同pH的HA、HB溶液,分别加水稀释相同的倍数后测定pH,pH变化大者酸性较强.
点评 本题考查弱电解质判断方法及实验方案设计,为高频考点,明确弱电解质电离特点是解本题关键,难点是实验方案设计,侧重考查学生实验设计及实验操作能力,题目难度中等.

CO2(g)+CH4(g)?2CO(g)+2H2(g)△H=+183.4kJ•mol-1
(1)已知该反应在一定条件下能自发进行,则下列说法正确的是②(填代号)
①该反应△S>0,反应条件为低温;
②该反应△S>0,反应条件为高温;
③该反应△S<0,反应条件为低温;
④该反应△S<0,反应条件为高温
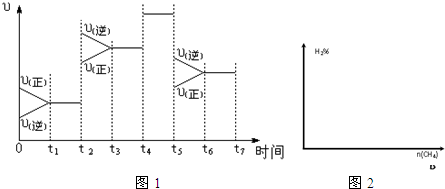
(2)如图1表示该反应在某一时间段中反应速率与反应过程的关系图(t2、t4、t5时刻改变的条件都只有一个,且各不相同).各阶段平衡时对应的平衡常数如表所示:
| t1~t2 | t3~t4 | t4~t5 | t6~t7 |
| K1 | K2 | K3 | K4 |
(3)若该反应在某恒温恒容容器中进行,加入一定量的CO2,在图2中画出随起始CH4物质的量增加,平衡时H2百分含量的变化曲线.
(4)某温度下,向1L恒容密闭容器中通入1mol CO2、1mol CH4,发生如下反应:CO2(g)+CH4(g)?2CO(g)+2H2(g).3分钟后达平衡,测得CH4体积分数为25%,CO2转化率为α.
①3分钟内用氢气表示的化学反应速率为V(H2)=0.22mol•L-1•min-1,CO2转化率为α=0.33(结果均保留两位有效数字).
②其他条件不变,改为加入3mol CO2、3mol CH4,平衡时CO2的转化率会小于α.(填“大于”、“小于”、“等于”或“无法判断”)
③其他条件不变,如果起始时各物质的浓度如表
| 物质 | CO2 | CH4 | CO | H2 |
| 浓度(mol•L-1) | 1 | 1 | 1 | 1 |
| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |

填写下列空白:
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应.写出A中所发生反应的化学方程式(有机物写结构简式):
 .
.(2)试管C中苯的作用是除去溴化氢中混有的溴蒸汽;反应开始后,观察D试管,看到的现象为石蕊试液变红,并在导管中有白雾产生
(3)在上述整套装置中,具有防倒吸作用的仪器有DEF(填字母).
(4)反应完毕后,将a瓶中的液体取出,经过分液 (填分离操作的名称)可获得获得粗溴苯,向粗溴苯中加入无水CaCl2,其目的是干燥
(5)经以上分离操作后,要进一步提纯粗溴苯,下列操作中必须的是C(填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取.
| 弱酸化学式 | H2SO3 | H2CO3 |
| 电离常数(25℃) | Ka1=1.3×10-2 Ka2=6.3×10-8 | Ka1=4.2×10-7 Ka2=5.6×10-11 |
关于两溶液的比较下列说法正确的是( )
| A. | c(HCO3-)<c(CO32-) | |
| B. | 两溶液都能使酸性高锰酸钾溶液褪色 | |
| C. | c(HCO3-)>c(HSO3-) | |
| D. | c(CO32-)+c(HCO3-)=c(SO32-)+c(HSO3-) |
①苯酚溶液加热变澄清
②苯酚浊液中加NaOH后,溶液变澄清,生成苯酚钠和水
③苯酚可与FeCl3反应
④在苯酚溶液中加入浓溴水产生白色沉淀
⑤苯酚钠溶液中通入CO2,出现浑浊
⑥苯酚能与Na2CO3溶液反应放出CO2.
| A. | ②⑤ | B. | ⑤ | C. | ③④⑥ | D. | ③④⑤ |
| A. | 醋酸的电离度 | B. | 溶液的导电性 | ||
| C. | 溶液的c(OH-) | D. | 溶液中$\frac{[C{H}_{3}COO].[{H}^{+}]}{[C{H}_{3}COOH]}$ |
 氯元素是生产生活中常见的非金属元素
氯元素是生产生活中常见的非金属元素