题目内容
6. 将海水淡化后,从剩余的浓海水中通过一系列工艺流程可以生产其他产品.
将海水淡化后,从剩余的浓海水中通过一系列工艺流程可以生产其他产品.(1)Cl2可以氧化浓海水中的Br-,用空气吹出Br2,并用纯碱吸收.纯碱吸收溴的主要反应是Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(化学方程式未配平),则吸收1mol Br2时,该反应转移的电子为$\frac{5}{3}$mol.
(2)精制浓海水可以得到纯净的饱和食盐水,向其中加入碳酸氢铵可制备碳酸氢钠.
①NaCl的电子式是
 .
.②上述制备碳酸氢钠的化学方程式是NaCl+NH4HCO3═NaHCO3↓+NH4Cl.
③为测定制得的碳酸氢钠的纯度,可称量a g碳酸氢钠样品(含少量NaCl)溶于足量盐酸,蒸干溶液后灼烧,剩余固体质量为b g.样品碳酸氢钠的质量分数是$\frac{84(a-b)}{25.5a}$×100%(用含a、b的代数式表示).
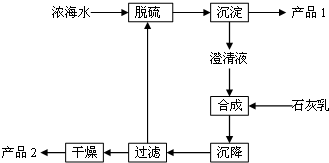
(3)海水提取镁的一段工艺流程如图:
浓海水中的有关成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g•L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
②产品2的化学式为Mg(OH)2;1L浓海水最多可得到产品2的质量为69.6 g.
分析 (1)一般用氯气或过氧化氢氧化Br-,反应Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3中,Br元素化合价分别由0价变化为-1价、+5价,结合化合价的变化计算;
(2)①氯化钠是离子化合物,钠离子和氯离子形成离子键;
②纯净的饱和食盐水,利用溶解度的不同,向其中加入碳酸氢铵可制备碳酸氢钠.
③称量a g碳酸氢钠样品(含少量NaCl)溶于足量盐酸,蒸干溶液后灼烧,剩余固体质量为b g,设碳酸氢钠物质的量为x,含氯化钠物质的量为y,依据元素守恒列式计算,NaHCO3+HCl=NaCl+H2O+CO2↑,
84x+58.5y=a
(x+y)×58.5=b
计算得到xy,碳酸氢钠的质量分数等于碳酸氢钠质量除以混合物总质量;
(3)工艺流程合成步骤中加入石灰乳,沉降后,将过滤后的滤液进行脱硫,应是用钙离子沉淀硫酸根离子生成硫酸钙沉淀,产品1为硫酸钙,合成得到氢氧化镁沉淀,故过滤后干燥的产品2为氢氧化镁,计算1L溶液中Mg2+的质量,根据Mg2+~Mg(OH)2计算氢氧化镁的质量;
解答 解:(1)一般用氯气或过氧化氢氧化Br-,反应Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3中,Br元素化合价分别由0价变化为-1价、+5价,反应中Br2起氧化剂、还原剂作用,根据电子转移守恒可知,2×n氧化剂(Br2)=2×5×n还原剂(Br2),故n氧化剂(Br2):n还原剂(Br2)=5:1,故吸收1mol Br2时,转移的电子数为1mol×2×$\frac{1}{1+5}$×5=$\frac{5}{3}$mol,
故答案为:$\frac{5}{3}$;
(2)①氯化钠是离子化合物,是钠离子和氯离子通过静电作用形成的,其电子式为 ,
,
故答案为: ;
;
②纯净的饱和食盐水,利用溶解度的不同,向其中加入碳酸氢铵可制备碳酸氢钠,反应的化学方程式为:NaCl+NH4HCO3═NaHCO3↓+NH4Cl,
故答案为:NaCl+NH4HCO3═NaHCO3↓+NH4Cl;
③量a g碳酸氢钠样品(含少量NaCl)溶于足量盐酸,蒸干溶液后灼烧,剩余固体质量为b g,设碳酸氢钠物质的量为x,含氯化钠物质的量为y,依据元素守恒列式计算,NaHCO3+HCl=NaCl+H2O+CO2↑,
84x+58.5y=a
(x+y)×58.5=b
x=$\frac{a-b}{25.5}$mol
样品碳酸氢钠的质量分数=$\frac{\frac{a-b}{25.5}mol×84g/mol}{ag}$×100%=$\frac{84(a-b)}{25.5a}$×100%,
故答案为:$\frac{84(a-b)}{25.5a}$×100%,
(3)①工艺流程合成步骤中加入石灰乳,沉降后,将过滤后的滤液进行脱硫,用Ca2+沉淀SO42-生成CaSO4沉淀,离子方程式为:Ca2++SO42-=CaSO4↓,
故答案为:Ca2++SO42-═CaSO4↓:
②采用过滤的方法得到产品1为CaSO4,滤液中加入石灰乳,发生反应为Mg2++2OH-=Mg(OH)2↓,合成中应得到Mg(OH)2沉淀,过滤、干燥的产品2为Mg(OH)2,
溶液中m(Mg2+)=1L×28.8g/L=28.8g,
Mg2+~Mg(OH)2
24g 58g
28.8g m[Mg(OH)2]
m[Mg(OH)2]=28.8g×$\frac{58g}{24g}$=69.6g,
故答案为:Mg(OH)2;69.6;
点评 本题考查了物质性质的分析应用,主要是氧化还原反应电子转移的计算,化学方程式计算,混合物成分的纯度计算应用,掌握物质性质和计算方法是解题关键,题目难度中等.

 名校课堂系列答案
名校课堂系列答案| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |

填写下列空白:
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应.写出A中所发生反应的化学方程式(有机物写结构简式):
 .
.(2)试管C中苯的作用是除去溴化氢中混有的溴蒸汽;反应开始后,观察D试管,看到的现象为石蕊试液变红,并在导管中有白雾产生
(3)在上述整套装置中,具有防倒吸作用的仪器有DEF(填字母).
(4)反应完毕后,将a瓶中的液体取出,经过分液 (填分离操作的名称)可获得获得粗溴苯,向粗溴苯中加入无水CaCl2,其目的是干燥
(5)经以上分离操作后,要进一步提纯粗溴苯,下列操作中必须的是C(填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取.
| A. | Na2O、Na2O2为相同元素组成的金属氧化物,都属于碱性氧化物 | |
| B. | SiO2、CO2均为酸性氧化物,均能与NaOH溶液反应生成盐和水 | |
| C. | FeO、Fe2O3均为碱性氧化物,与氢碘酸反应均只发生复分解反应 | |
| D. | 将Fe(OH)3胶体和泥水分别进行过滤,分散质均不能通过滤纸孔隙 |
| Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.143 |
| 主要化合价 | -2 | -1,+7 | +3 |
| A. | X与M形成的化合物中含有离子键 | |
| B. | Z、M、Q三种元素的简单离子的半径:M>Z>Q | |
| C. | Y与R形成的化合物中R呈正价,说明Y的非金属性比R强 | |
| D. | 在元素周期表中,Q位于金属与非金属的交界处,可以作半导体材料 |
| A. | HCl | B. | Na | C. | Na2SO4 | D. | NaHSO4 |
反应 I:CO(g)+2H2(g)?CH3OH(g)△H1
反应 II:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2
①上述反应符合“原子经济”原则的是I(填“I”或“II”)
②下表所列数据是反应 I 在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
③某温度下,将 2 mol CO 和 6 mol H2 充入 2L 的密闭容器中,充分反应,达到平衡后,测 得 c(CO)=0.2 mol/L,则 CO 的转化率为80%,此时的温度为250℃(从表中选择).
| A. | 表示物质数量的单位 | |
| B. | 用巨大数量的微粒集体表示物质的量的单位 | |
| C. | 表示物质的质量单位 | |
| D. | 既表示物质的质量又表示物质微粒的数量单位 |
 氯元素是生产生活中常见的非金属元素
氯元素是生产生活中常见的非金属元素