题目内容
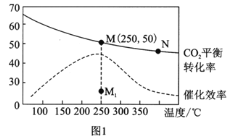
【题目】已知难溶性物质K2SO4·MgSO4·2CaSO4在水中存在如下平衡:K2SO4·MgSO4·2CaSO4 (s)![]() 2Ca2++2K++Mg2++4SO42-。不同温度下,K+的浸出浓度与溶浸时间的关系如图所示,则下列说法错误的是
2Ca2++2K++Mg2++4SO42-。不同温度下,K+的浸出浓度与溶浸时间的关系如图所示,则下列说法错误的是
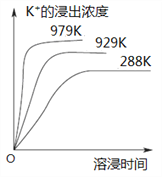
A.该平衡的Ksp=c2(Ca2+)·c2(K+)·c(Mg2+)·c4(SO42-)B.向该体系中加入饱和K2SO4溶液,溶解平衡向左移动 C.升高温度,溶浸速率增大,平衡向正反应方向移动 D.向该体系中加入饱和NaOH溶液,溶解平衡不发生移动
【答案】D
【解析】
根据沉淀溶解平衡,K2SO4·MgSO4·2CaSO4 (s)![]() 2Ca2++2K++Mg2++4SO42-,该平衡的Ksp=c2(Ca2+)·c2(K+)·c(Mg2+)·c4(SO42-) ,故A正确;向该体系中加入饱和K2SO4溶液,增大c(SO42-),溶解平衡向左移动,故B正确;根据图像得出,温度越高,钾离子的浓度越大,说明升高温度,平衡向右移动,故C正确;向该体系中加入饱和氢氧化钠溶液时,氢氧根离子与镁离子反应生成难溶的氢氧化镁沉淀,降低了镁离子的浓度,使平衡向右移动,故D错误。
2Ca2++2K++Mg2++4SO42-,该平衡的Ksp=c2(Ca2+)·c2(K+)·c(Mg2+)·c4(SO42-) ,故A正确;向该体系中加入饱和K2SO4溶液,增大c(SO42-),溶解平衡向左移动,故B正确;根据图像得出,温度越高,钾离子的浓度越大,说明升高温度,平衡向右移动,故C正确;向该体系中加入饱和氢氧化钠溶液时,氢氧根离子与镁离子反应生成难溶的氢氧化镁沉淀,降低了镁离子的浓度,使平衡向右移动,故D错误。

【题目】中国科学家创造性地构建了硅化物晶格限域的单铁中心催化剂,成功地实现了甲烷在无氧条件下选择活化,一步高效生产乙烯、芳烃和氢气等化学品。请回答下列问题:
(1)基态铁原子的价层电子轨道表达式为______。
(2)硅、碳位于同一主族,用“![]() ”“
”“![]() ”或“
”或“![]() ”填空:
”填空:
性质 | 原子半径 | 第一电离能 | 熔点 | 键能 |
项目 |
|
|
|
|
(3)CN-能与Fe3+形成配合物,与CN-互为等电子体的分子有______ (任写一种);1 mol[Fe(CN)6 ]3-中含______molσ键。
(4)已知:反应![]() ,碳原子的杂化类型转化过程为______;
,碳原子的杂化类型转化过程为______;
从共价键重叠方式看,![]() 分子中
分子中![]() 键类型为;
键类型为;![]() 的键角比
的键角比![]() 的键角______
的键角______![]() 填“大”或“小”
填“大”或“小”![]() 。
。
(5)晶体有两种晶胞,如图1、图2所示。

图1中晶胞中铁的配位数为______;图2中铁晶胞堆积方式为______。
(6)碳化硅晶胞如图3所示,已知碳化硅晶体的密度为dgcm-3,NA表示阿伏加德罗常数的值,则碳化硅中硅碳键的键长为______ pm。