题目内容
6.下列反应离子方程式书写正确的是( )| A. | 钠和冷水反应:Na+2H2O═Na++OH-+H2↑ | |
| B. | 金属铝溶于氢氧化钠:Al+2OH-═AlO2-+H2↑ | |
| C. | 金属铝溶于盐酸中2Al+6H+═2Al3++3H2↑ | |
| D. | 铁跟稀盐酸反应:Fe+2H+═Fe3++H2↑ |
分析 A.原子个数不守恒;
B.电荷数不守恒;
C.铝与盐酸反应生成氯化铝和氢气;
D.铁与稀盐酸反应生成二价铁离子和氢气.
解答 解:A.钠和冷水反应,离子方程式:2Na+2H2O═2Na++2OH-+H2↑,故A错误;
B.金属铝溶于氢氧化钠溶于:2Al+2H2O+2OH-═2AlO2-+3H2↑,故B错误;
C.金属铝溶于盐酸中,反应生成氯化铝和氢气,离子方程式为:2Al+6H+═2Al3++3H2↑,故C正确;
D.铁跟稀盐酸反应,生成氯化亚铁和氢气,离子方程式:Fe+2H+═Fe2++H2↑,故D错误;
故选:C.
点评 本题考查了离子方程式的书写,明确反应的实质是解题关键,注意离子方程式书写应遵循客观事实、遵循原子个数、电荷数守恒规律,题目难度不大.

练习册系列答案
相关题目
17.某有机物1.6g在足量的氧气中燃烧后测得生成二氧化碳的质量为4.4g,水的质量为3.6g则( )
| A. | 有机物一定含C,H元素,可能含氧元素 | |
| B. | 有机物只含C,H元素 | |
| C. | 有机物含C,H,O元素 | |
| D. | 此有机物化学式为CH4 |
1.在m A+n B?p C的反应中,m、n、p为各物质的计量数.现测得C每分钟增加a mol/L,B每分钟减少1.5a mol/L,A每分钟减少0.5a mol/L,则m:n:p为( )
| A. | 2:3:2 | B. | 2:3:3 | C. | 1:3:2 | D. | 3:1:2 |
11.下列反应的离子方程式不正确的是( )
| A. | 锌与硫酸铜溶液反应:Zn+Cu2+═Zn 2++Cu | |
| B. | 氢氧化钠溶液与盐酸反应:OH-+H+═H2O | |
| C. | 铁与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 氯化钡溶液与稀硫酸反应:Ba2++SO42-═BaSO4 |
18.下列各组物质中化学键的类型相同的是( )
| A. | HCl、MgCl2 | B. | Na2O、CO2 | C. | CaCl2、CH4 | D. | NH3、H2O |
16.四种短周期元素的性质或结构信息如下表,下列结论中错误的是( )
| 元素 | W | X | Y | Z |
| 性质或结构信息 | 单质制成的高压灯,发出的黄光透雾力强、射程远. | 工业上通过分离液态空气获得其单质.原子的最外层未达到稳定结构. | 单质常温常压下是气体,原子的M层差一个电子达稳定结构. | +2价阳离子的核外电子排布与氖原子相同. |
| A. | 上表中与W属于同一周期的元素是Z和Y | |
| B. | Z和Y形成的化合物属于离子化合物 | |
| C. | X的氢化物常温、常压下一定为液体 | |
| D. | Y单质为有色气体,具有强氧化性 |
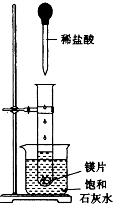 如图所示,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.试回答下列回答:
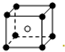
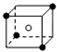
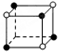
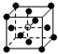
如图所示,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.试回答下列回答: 和化学式中M分别代表阳离子,图中
和化学式中M分别代表阳离子,图中 和化学式中N分别代表阴离子,则化学式为MN的晶体结构为( )
和化学式中N分别代表阴离子,则化学式为MN的晶体结构为( )