题目内容
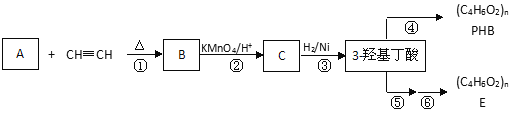
【题目】3-羟基丁酸(3-hydroxybutyrate)也称为β-羟基丁酸(beta-hydroxybutyrate),在工业中可用于合成可生物降解的塑料,如聚(3-羟基丁酸)。
已知:i. 共轭二烯烃(如异戊二烯)与含有碳碳叁键的有机物作用时能形成环状化合物:
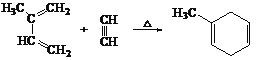
ii. 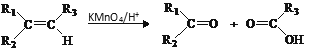
iii. 步骤②只有一种产物;E的结构中含有甲基
(1)A分子结构简式 _______;理论上B也可以由1,3-丁二烯与烃F来合成,则F的名称(系统命名法):_________;C中含有的官能团是_______(用符号表示)。
(2)写出反应类型:②_____________, ④_____________。
(3)PHB______(填“有”或“无”)固定熔沸点;它与E______(填“互为”或“不互为”)同分异构体。下列有机物具有类似共轭二烯烃性质的是__________(填序号);
a. ![]() b.
b. ![]()
c. ![]() d.
d. 
(4)写出反应⑤的化学方程式________。
【答案】 2-丁炔
2-丁炔 ![]() 、-COOH 氧化 缩聚 无 不互为 bd CH3CH(OH)CH2COOH
、-COOH 氧化 缩聚 无 不互为 bd CH3CH(OH)CH2COOH![]() CH3CH=CHCOOH+H2O
CH3CH=CHCOOH+H2O
【解析】
由转化关系可知,B发生信息ii反应生成C,C与氢气发生反应生成3-羟基丁酸,逆推可得C为CH3COCH2COOH,A与CH≡CH发生信息i反应生成B,则B为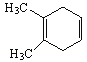 ,A为
,A为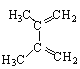 。3-羟基丁酸也可以通过两步反应形成另一种高聚物E,则应先发生消去反应生成CH3CH=CHCOOH,CH3CH=CHCOOH发生加聚反应得到E,故E为
。3-羟基丁酸也可以通过两步反应形成另一种高聚物E,则应先发生消去反应生成CH3CH=CHCOOH,CH3CH=CHCOOH发生加聚反应得到E,故E为![]() ;故3-羟基丁酸通过酯化反应进行的缩聚反应反应生成PHB,则PHB为
;故3-羟基丁酸通过酯化反应进行的缩聚反应反应生成PHB,则PHB为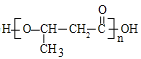 ,据此解答。
,据此解答。
根据上述分析可知:A为 ,B为
,B为 ,C为CH3COCH2COOH,E为
,C为CH3COCH2COOH,E为![]() ,PHB为
,PHB为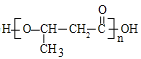 。
。
(1)由上述分析可知,A为 ,B为
,B为 ,可以由1,3-丁二烯与CH3C≡CCH3通过加成反应合成,所以F为CH3C≡CCH3,F的名称2-丁炔;C为CH3COCH2COOH,含有的官能团是
,可以由1,3-丁二烯与CH3C≡CCH3通过加成反应合成,所以F为CH3C≡CCH3,F的名称2-丁炔;C为CH3COCH2COOH,含有的官能团是![]() 、-COOH;
、-COOH;
(2)反应②B: 与酸性KMnO4溶液反应产生C:CH3COCH2COOH,所以反应类型属于氧化反应,反应④是CH3CH(OH)CH2COOH与浓硫酸共热发生反应产生PHB:
与酸性KMnO4溶液反应产生C:CH3COCH2COOH,所以反应类型属于氧化反应,反应④是CH3CH(OH)CH2COOH与浓硫酸共热发生反应产生PHB: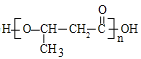 ,同时产生H2O,反应类型为缩聚反应;
,同时产生H2O,反应类型为缩聚反应;
(3)PHB为混合物,没有固定的熔点;PHB与E都属于高聚物,但n值不同,二者不是同分异构体;碳碳双键双键通过碳碳单键连接,具有类似共轭二烯烃性质。
a.苯中不含不饱和键,不具有类似共轭二烯烃性质,a不符合题意;
b.![]() 中存在碳碳双键通过碳碳单键连接,具有类似共轭二烯烃性质,b符合题意;
中存在碳碳双键通过碳碳单键连接,具有类似共轭二烯烃性质,b符合题意;
c.![]() 中不存在碳碳双键通过碳碳单键连接,不具有类似共轭二烯烃性质,c不符合题意;
中不存在碳碳双键通过碳碳单键连接,不具有类似共轭二烯烃性质,c不符合题意;
d.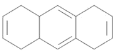 中存在碳碳双键通过碳碳单键连接,具有类似共轭二烯烃性质,d符合题意;
中存在碳碳双键通过碳碳单键连接,具有类似共轭二烯烃性质,d符合题意;
故合理选项是bd;
(4)反应⑤为3-羟基丁酸与浓硫酸混合加热发生消去反应产生CH3CH=CHCOOH和水,反应方程式为:CH3CH(OH)CH2COOH![]() CH3CH=CHCOOH+H2O。
CH3CH=CHCOOH+H2O。

 阅读快车系列答案
阅读快车系列答案【题目】有三种镁铝合金样品(组分比例不一定相同)①、②、③。小奉、小贤、小红三同学各取一种样品,对合金中镁的质量分数进行下列实验探究:
(1)小奉取样品①m1 g和过量的氢氧化钠溶液反应,然后过滤;再往滤液中通入过量的二氧化碳气体,将所得沉淀过滤、洗涤、烘干、灼烧,得到固体质量仍为m1 g。则合金中镁的质量分数为___________。(保留小数点后面2位)
(2)小贤取样品②m2 g和足量的稀硫酸反应,发现固体完全溶解,标准状况下得到气体体积为VL,则m2的取值范围是_________。(结果转化为最简分数)
(3)小红取不同质量的样品③分别和30 mL同浓度的盐酸反应,所取合金质量与产生气体的体积(标准状况下测定)如下所示:
实验序号 | a | b | c |
合金质量(g) | 0.51 | 0.765 | 0.918 |
气体体积(mL) | 560 | 672 | 672 |
求:I.盐酸的物质的量浓度_______
II.合金中镁的质量分数_______
III.要使c组实验后剩余合金中的铝恰好完全溶解,还需向容器中加入1.0 mol/L的氢氧化钠溶液多少mL_______?
【题目】硝酸铝是一种常用皮革鞣剂.工业上用铝灰(主要含Al、A12O3、Fe2O3等)制取硝酸铝晶体[Al(NO3)3﹒nH2O]的流程如下:
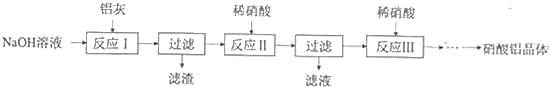
完成下列填空:
(1)用NaOH固体配制30%的NaOH溶液,所需的玻璃仪器除烧杯外,还有______。
a.容量瓶 b.量筒 c.烧瓶
(2)反应Ⅱ中为避免铝的损失,需要解决的问题是______。
(3)从反应Ⅲ所得溶液中得到硝酸铝晶体的步骤依次是:减压蒸发、______、过滤、______、低温烘干.
(4)有人建议将反应Ⅱ、Ⅲ合并以简化操作,说明工业上不采用这种方法的原因______。
(5)某同学在实验室用铝灰制各硝酸铝晶体,其流程如下:
氢氧化物 | Fe(OH)3 | Al(OH)3 |
开始沉淀pH | 1.9 | 4.2 |
沉淀完全pH | 3.2 | 5.4 |
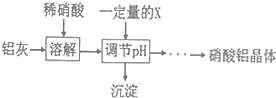
调节pH的目的是______,为使得到的硝酸铝晶体较纯净,所用的X物质可以是______(填编号)。
A.氨水 B.铝 c.氢氧化铝 D.偏铝酸钠
(6)该实验室制法与工业上制法相比,其缺点是______。
(7)称取7.392g硝酸铝晶体样品,加热灼烧使其分解完全,最终得到1.020gAl2O3,计算硝酸铝晶体样品中结晶水的数目为______。