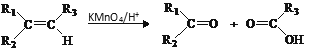
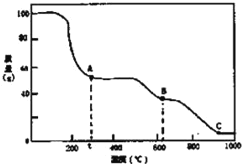
题目内容
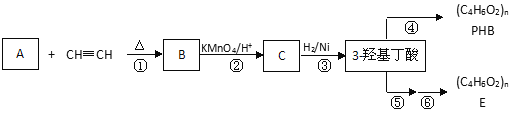
【题目】饱和二氧化硫水溶液中存在下列平衡体系:SO2+H2O![]() H++HSO3﹣ HSO3﹣
H++HSO3﹣ HSO3﹣![]() H++SO32﹣,若向此溶液中( )
H++SO32﹣,若向此溶液中( )
A.加水,SO32﹣浓度增大
B.通入少量Cl2气体,溶液pH增大
C.加少量CaSO3粉末,HSO3﹣浓度基本不变
D.通入少量HCl气体,溶液中HSO3﹣浓度减小
【答案】D
【解析】
A.加水稀释,虽然平衡正向移动,但达平衡时,SO32﹣浓度仍减小,故A错误;
B.氯气与将亚硫酸反应,生成硫酸和盐酸,溶液中氢离子浓度增大,溶液pH减小,故B错误;
C.CaSO3与H+反应生成HSO3-,从而增大溶液中的HSO3﹣浓度,故C错误;
D.通入HCl气体,氢离子浓度增大,第一步电离平衡逆向移动,HSO3﹣浓度减小,故D正确;
故选D。

【题目】氮的氧化物是严重的大气污染物,可以通过以下方法处理:
Ⅰ.催化还原法:如在汽车排气管上安装一个催化转化器,发生如下反应: 2NO(g)+2CO(g)N2(g)+2CO2(g)
(1)已知N2(g)+O2(g)2NO(g) △H=+180kJ/mol
化学键 | O=O | C=O | C≡O |
键能(kJ/mol) | 497 | 803 | 1072 |
则反应:2NO(g)+2CO(g) N2(g)+2CO2(g) △H=_____kJ/mol。
(2)在一定温度下,向体积为1L的密闭容器中充入2molNO、1molCO,10分钟时反应2NO(g)+2CO(g)N2(g)+2CO2(g)达到平衡状态,反应过程中反应物浓度随时间变化情况如图所示:
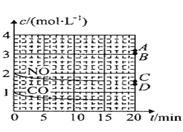
①该反应的平衡常数 K 的计算式为_____;前 10 分钟内用氮气表示的反应速率为_____。
②若保持温度不变,15 分钟时再向该容器中充入1.6molNO、0.4molCO2,则此时反应的ν正______ν逆(填“>”、“=”或“<”)。
③若保持其他条件不变,15min 时压缩容器的体积至 0.5L,20 分钟时反应重新达到平衡,NO 的浓度对应的点应是图中的_____(填字母)。
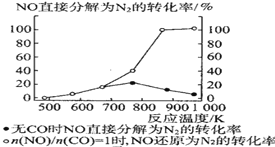
④某科研小组研究发现以 Ag-ZSM-5 为催化剂,NO 转化为 N2 的转化率随温度变化情况如图所示。若不使用 CO,温度超过775K,发现NO的分解率降低,其可能的原因是__________________
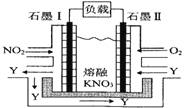
Ⅱ.利用电化学原理,将 NO2、O2和熔融 KNO3制成燃料电池,其原理如图,该电池在工作过程中NO2转变成绿色硝化剂Y,Y是一种氧化物,可循环使用,石墨Ⅰ附近发生的反应电极反应式为_____相同条件下,消耗的 O2和 NO2的体积比为_____