题目内容
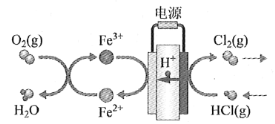
【题目】氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:

(1)反应Ⅰ的化学方程式是______________________________________
(2)已知反应Ⅱ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g) △H=+550 kJ·mol-1
它由两步反应组成:i.H2SO4(l)=SO3(g)+H2O(g) △H=+177 kJ·mol-1
ii.SO3(g)分解。
则SO3(g)分解的热化学方程式为____________________。
(3)L(L1、L2)、X可分别代表压强或温度其中之一。如图表示L一定时,ii中SO3(g)的质量分数随X的变化关系。

①X代表的物理量是__________。
②判断L1、L2的大小关系:L1_______L2,并简述理由:______________。
【答案】SO2+2H2O+I2=H2SO4+2HI 2SO3(g)2SO2(g)+O2(g) △H== + 196kJmol-1 温度 L1<L2 SO3(g)分解是体积增大的反应,当温度一定时,压强增大,SO3质量分数增大。
【解析】
(1)根据图中信息可知反应Ⅰ中反应物为SO2、H2O和I2,生成物为H2SO4和HI,根据氧化还原反应方程式的配平方法配平;
(2)根据反应Ⅱ和步骤ⅰ写出步骤ⅱ的热化学反应方程式为:2SO3(g)=2SO2(g)+O2(g)△H=+196KJmol-1;
(3)①该反应正反应为吸热反应,温度升高,平衡逆向移动,SO3的转化率减小,故X代表的物理量为温度;
②根据①可知L代表的物理量为压强。SO3(g)分解是体积增大的反应,当温度一定时,压强增大,SO3质量分数增大,故L2>L1。
(1)根据图中信息可知反应Ⅰ中反应物为SO2、H2O和I2,生成物为H2SO4和HI,故反应Ⅰ的化学方程式是SO2+2H2O+I2=H2SO4+2HI,故答案为:SO2+2H2O+I2=H2SO4+2HI。
(2)已知:①2H2SO4(l)═2SO2(g)+O2(g)+2H2O(g)△H=+550kJmol-1②H2SO4(l)═SO3(g)+H2O(g)△H=+177kJmol-1,根据盖斯定律①-2×②可得:2SO3(g)=2SO2(g)+O2(g)△H=+196kJ/mol;故答案为:2SO3(g)=2SO2(g)+O2(g)△H=+196kJ/mol。
(3)①该反应正反应为吸热反应,温度升高,平衡逆向移动,SO3的转化率减小,故X代表的物理量为温度,故答案为:温度。
②根据①可知L代表的物理量为压强。SO3(g)分解是体积增大的反应,当温度一定时,压强增大,SO3质量分数增大,故L2>L1,故答案为:L2>L1;SO3(g)分解是体积增大的反应,当温度一定时,压强增大,SO3质量分数增大。