题目内容
【题目】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位置、结构和性质的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
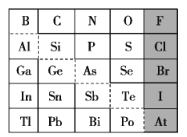
(1)Sn的最高价氧化物对应水化物的化学式为___,N、O、F对应的简单离子的半径由大到小的顺序为___。(写离子符号)
(2)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是___。(写化学式)
②H3AsO4、H2SeO4的酸性强弱:H3AsO4(填“>”“<”或“=”)___ H2SeO4。
③镓的氯化物与氨水反应的化学方程式为___。
(3)用铝和金属氧化物反应制备金属单质是工业上较常用的方法。如:2A1+4BaO![]() 3Ba↑+BaOA12O3
3Ba↑+BaOA12O3
利用上述方法可制取Ba的主要原因是(________)
a.高温时A1的活泼性大于Ba
b.高温有利于BaO分解
c.高温时BaOA12O3比Al2O3稳定
d.Ba的沸点比A1的低
(4)用铝热法还原下列氧化物,制得金属各1mo1,消耗铝最少的是___。
a.MnO2 b.WO3 c.Cr2O3 d.Co3O4
【答案】H2SnO3或Sn(OH)4或H4SnO4 N3->O2->F- HF < GaC13+3NH3H2O=Ga(OH)3↓+3NH4C1 d d
【解析】
(1)根据周期表可知,Sn与C同主族,则Sn的最高正价为+4价,其最高价氧化物对应水化物的化学式为H2SnO3或Sn(OH)4或H4SnO4,N、O、F对应的简单离子的核外电子层数相同,核电荷数N<O<F,则离子半径N3->O2->F-;
(2)①同一主族元素自上而下非金属性依次减弱,非金属性越强,氢化物的稳定性越强,则阴影部分元素氢化物热稳定性最高的是HF;
②非金属性越强,最高价氧化为对应水化物的酸性越强,非金属性Se>As,则酸性H3AsO4<H2SeO4;
③镓的氯化物为GaCl3,与氨水反应生成氯化铵和Ga(OH)3,反应的化学方程式为GaC13+3NH3H2O=Ga(OH)3↓+3NH4C1;
(3)Al在高温下可将氧化钡中钡置换出来,原因是Ba的沸点低于铝,高温时Ba转化为气体脱离反应体系,使反应正向进行,故选d;
(4)根据化合价的变化判断,化合价变化的数值越小,说明发生氧化还原反应时得到的电子数目越少,则消耗铝的量最少;
a.MnO2~Mn,生成1molMn,需要4mol电子,消耗![]() molAl;
molAl;
b.WO3~W,生成1molW,需要6mol电子,消耗2molAl;
c.Cr2O3~Cr,生成1molCr,需要3mol电子,消耗1molAl
d.Co3O4~Co,生成1molCo,需要![]() mol电子,消耗
mol电子,消耗![]() molAl;
molAl;
结合以上分析可知,消耗Al最少的是Co3O4,故答案选d。

【题目】某学习小组做了如下实验探究海带中碘元素的存在形式,探究过程如图:
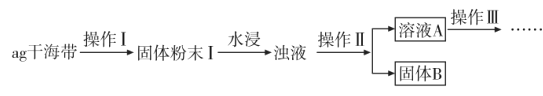
(1)操作I为灼烧,则灼烧时应该用___(仪器名称)盛装海带,操作II为___;
(2)水浸时通常要将悬浊液煮沸2-3min,目的是___。
(3)操作III,是同学们对溶液A中碘元素的存在形式进行的探究实验。
推测:①以IO![]() 形式存在②以I-形式存在
形式存在②以I-形式存在
查阅资料:IO![]() 具有较强的氧化性将上述溶液稀释配制成200mL溶液,请完成下列实验探究。
具有较强的氧化性将上述溶液稀释配制成200mL溶液,请完成下列实验探究。
限选试剂:3%H2O2溶液、KSCN溶液、FeC12溶液、稀硫酸
序号 | 实验操作 | 实验现象 | 结论 |
① | 取少量稀释后的溶液A加入淀粉后再 用硫酸酸化,分装于试管I、II | 无现象 | |
② | 往试管I中加入FeC12溶液,然后加入2滴KSCN溶液并振荡; | ___ | 证明不是以IO |
③ | 往试管II中加入___; | ____ | 证明以I-形式存在 |
(4)取20mL稀释后溶液A于锥形瓶,滴加0.01mo1/LKMnO4溶液至溶液刚显浅红色,将I-氧化为I2并得到溶液B;已知在酸性条件下,MnO![]() 的还原产物为Mn2+,写出离子方程式___。
的还原产物为Mn2+,写出离子方程式___。