题目内容
【题目】给某潜水器提供动力的电池如图所示。下列有关说法正确的是( )
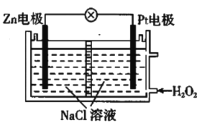
A.Zn极发生了还原反应
B.电池中的Na+向Zn电极移动
C.Pt电极反应式为H2O2+2e-=2OH-
D.电子从Zn电极沿导线流向Pt电极,再经溶液回到Zn电极
【答案】C
【解析】
锌、过氧化氢和食盐水形成原电池,锌作负极,电极反应为Zn-2e-=Zn2+,铂作正极,电极反应为H2O2+2e-=2OH-,电子从负极经导线流向正极,电解质溶液中阳离子移向正极,阴离子移向负极,据此分析。
A.锌作负极,电极反应为Zn-2e-=Zn2+,Zn极发生了氧化反应,故A错误;
B.阳离子向原电池的正极移动,电池中的Na+向Pt电极移动,故B错误;
C.铂作正极,Pt电极反应式为H2O2+2e-=2OH-,故C正确;
D.电子从负极移向正极,电子从Zn电极沿导线流向Pt电极,电子不能在溶液中流动,故D错误;
答案选C。

练习册系列答案
相关题目