题目内容
【题目】一定条件下反应2SO2(g)+O2(g)![]() 2SO3(g)在恒容密闭容器中进行,从反应开始至10s时,O2的浓度减少了0.3mol/L则,0~10s内平均反应速率为
2SO3(g)在恒容密闭容器中进行,从反应开始至10s时,O2的浓度减少了0.3mol/L则,0~10s内平均反应速率为
A. v(O2)=0.3mol.L-1.s-1B. v(O2)=0.03mol.L-1.s-1
C. v(SO2)=0.03mol.L-1.s-1D. v(SO3)=0.03mol.L-1.s-1
【答案】B
【解析】
先根据10s内氧气浓度的变化计算氧气的反应速率,然后根据速率比等于化学计量数的比计算v(SO2)、v(SO3),进行判断。
A.从反应开始至10s时,O2的浓度减少了0.3mol/L,则用氧气的浓度变化表示反应速率v(O2)=![]() =0.03mol/(L·s),选项A错误,选项B正确;
=0.03mol/(L·s),选项A错误,选项B正确;
由于同一化学反应,用不同物质表示的反应速率,速率比等于化学计量数的比,则v(SO2):v(O2):v(SO3)=2:1:2,因此v(SO3)=v(SO2)=2v(O2)=0.06 mol/(L·s),选项C、D错误;
故合理选项是B。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
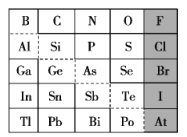
【题目】下表为元素周期表的一部分,针对表中①~⑧元素,回答下列问题
① | |||||||||||||||
② | ③ | ④ | |||||||||||||
⑤ | ⑥ | ⑦ | ⑧ |
(1)③元素在周期表中的位置是第二周期第_____________族
(2)写出②的最高价氧化物的电子式_____________
(3)⑤和⑥两种元素的最高价氧化物对应水化物中碱性较强的是_____________(填化学式)
(4)写出③和⑦的常见氢化物中稳定性较好的的物质的电子式_____________
(5)写出⑤⑧的最高价氧化物对应水化物互相反应的离子方程式_____________