题目内容
【题目】A+、B+、C-、D、E五种粒子(分子或离子)中,每个粒子均有10个电子,已知:
①A++C-![]() D+E↑;②B++C-===2D。
D+E↑;②B++C-===2D。
请回答:
(1)C-离子的电子式是________________。
(2)A+离子中的键角为______________。
(3)分别写出A+和D反应、B+和E反应的离子方程式____________、____________。
(4)除D、E外,请再写出两种含10个电子的分子的分子式____________。
(5)除A+、B+外,请再写出两种含10个电子的阳离子________。
【答案】![]() 109.5° NH4++H2O
109.5° NH4++H2O![]() NH3·H2O+H+ H3O++NH3=NH4++H2O CH4、Ne Na+、Mg2+
NH3·H2O+H+ H3O++NH3=NH4++H2O CH4、Ne Na+、Mg2+
【解析】
10电子微粒有:H2O、NH3、CH4、HF、NH4+、H3O+、OH-、Al3+、Na+、Mg2+、O2-、F-等;
根据:A++C-![]() D+E↑;②B++C-===2D可知A+为NH4+、B+为H3O+、C-为OH-、D为H2O、E为NH3,据此解答。
D+E↑;②B++C-===2D可知A+为NH4+、B+为H3O+、C-为OH-、D为H2O、E为NH3,据此解答。
(1)根据上述分析,C-的电子式为![]() ,
,
故答案为:![]() ;
;
(2)NH4+离子中的键角为109.5°,
故答案为:109.5°;
(3)A+和D反应的离子方程式为NH4++H2O![]() NH3·H2O+H+,B+和E反应的离子方程式H3O++NH3=NH4++H2O,
NH3·H2O+H+,B+和E反应的离子方程式H3O++NH3=NH4++H2O,
故答案为:NH4++H2O![]() NH3·H2O+H+;H3O++NH3=NH4++H2O;
NH3·H2O+H+;H3O++NH3=NH4++H2O;
(4)除H2O、NH3外,另外两种含10个电子的分子有:CH4、Ne、HF等,
故答案为:CH4、Ne;
(5)除NH4+,H3O+外,另外两种含10个电子的阳离子有:Na+、Mg2+、Al3+等,
故答案为:Na+、Mg2+。

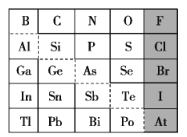
【题目】元素周期表是学习化学的重要工具,它隐含着许多信息和规律。如图是元素周期表的一部分,表中所列序号①、②、③、④、⑤、⑥、⑦、⑧分别代表某种化学元素。根据表格所给信息,回答下列问题:
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ||||||
3 | ⑤ | ⑥ | ⑦ | ④ | ⑧ | |||
(1)8种元素中,性质最稳定的是___(填元素符号)。
(2)①与④可形成___化合物(填“共价”、“离子”),其电子式为___。
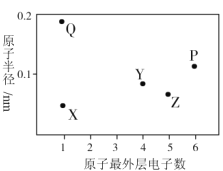
(3)原子半径②___③,①___⑤(填“>”、“<”或“=”)。
(4)在元素⑤、⑥、⑦中,金属性最强的元素是___。(填元素符号)。