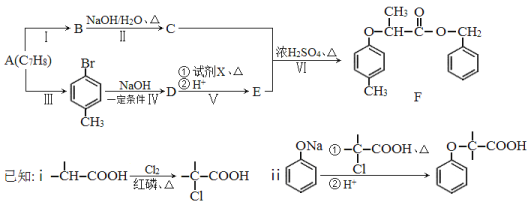
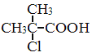题目内容
【题目】(1) 25℃时,物质的量浓度均为0.1mol/L的下列四种溶液:
① Na2CO3溶液 ② NaHCO3溶液 ③ NaF溶液 ④NaClO溶液。依据数据判断pH由大到小的顺序是_________________________。
(2)清除水瓶水垢中含有的CaSO4的方法是:将水瓶中的水垢用碳酸钠饱和溶液浸泡后加水冲洗,再加入盐酸即可,请写出上述反应的化学方程式:________________、_____________ 。
(3)Na2CO3溶液显碱性是因为CO32-水解的缘故,请设计简单的实验事实证明之____________________。
(4)电离平衡常数(用K表示)是一种平衡常数。电离平衡常数的大小可以判断电解质的相对强弱。25℃时,有关物质的电离平衡常数如下表所示:
化学式 | HF | H2CO3 | HClO |
电离平衡常数(K) | 7.2×10-4 | K1=4.4×10-7 K2=4.7×10-11 | 3.0×10-8 |
氢氟酸的电离方程式为____________________,次氯酸电离平衡常数的表达式为_______________。
(5)25℃时,pH=3的HF溶液中,未电离的氟化氢物质的量浓度为_______________________mol/L。
【答案】 ①>④>②>③ CaSO4(s)+CO32-(aq)![]() CaCO3(s)+SO42-(aq) CaCO3+2HCl
CaCO3(s)+SO42-(aq) CaCO3+2HCl![]() CaCl2+H2O+CO2↑ 取少量碳酸钠溶液,滴加1-2滴酚酞,溶液变红。再滴加氯化钙溶液,产生白色沉淀,红色消失 HF
CaCl2+H2O+CO2↑ 取少量碳酸钠溶液,滴加1-2滴酚酞,溶液变红。再滴加氯化钙溶液,产生白色沉淀,红色消失 HF![]() H++F- K=c(H+)·c(ClO-)/c(HClO) 1.4×10-3
H++F- K=c(H+)·c(ClO-)/c(HClO) 1.4×10-3
【解析】(1)酸性是HF>H2CO3>HClO>HCO3-,酸性越弱,相应的酸根越容易水解,溶液的碱性越强,因此① Na2CO3溶液、② NaHCO3溶液、 ③ NaF溶液、④NaClO溶液中pH由大到小的顺序是①>④>②>③。(2)碳酸钙的溶解度小于硫酸钙,因此沉淀容易转化为碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,所以反应的方程式分别是CaSO4(s)+CO32-(aq)=CaCO3(s)+SO42-(aq)、CaCO3+2HCl=CaCl2+H2O+CO2↑。(3)为证明纯碱溶液呈碱性是由CO32-引起的,可设计一个使溶液中的碳酸根离子由有到无的实验,根据溶液中酚酞颜色的变化判断,所以设计的实验为:在碳酸钠溶液中滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去或变浅,则说明Na2CO3溶液显碱性是因为CO32-水解的缘故;(4)氢氟酸是弱酸,电离方程式为HF![]() H++F-,根据次氯酸的电离方程式HClO
H++F-,根据次氯酸的电离方程式HClO![]() H++ClO-可知次氯酸电离平衡常数的表达式为K=c(H+)·c(ClO-)/c(HClO)。(5)25℃时,pH=3的HF溶液中氢离子浓度是0.001mol/L,根据电离方程式可知氟离子浓度也是0.001mol/L,所以根据电离平衡常数可知未电离的氟化氢物质的量浓度为
H++ClO-可知次氯酸电离平衡常数的表达式为K=c(H+)·c(ClO-)/c(HClO)。(5)25℃时,pH=3的HF溶液中氢离子浓度是0.001mol/L,根据电离方程式可知氟离子浓度也是0.001mol/L,所以根据电离平衡常数可知未电离的氟化氢物质的量浓度为![]() mol/L。
mol/L。

【题目】实验室用密度为1.19g/mL、质量分数为36.5%的浓盐酸配制230ml,1mol/L的盐酸。请回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为________,配制230ml,1mol/L的盐酸。
应量取浓盐酸的体积/mL | 实验需要的玻璃仪器(除烧杯、量筒) |
________ | ________ |
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是____。
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(3)配制时,正确的操作顺序是(用字母表示,每个字母只能用一次)_____。
A.用30mL蒸馏水洗涤烧杯2-3次,洗涤液均注入容量瓶中,振荡
B.用量筒准确量取所需的浓盐酸,沿玻璃棒倒入烧杯中,再加入少量蒸馏水(35mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入所选容积的容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管滴加蒸馏水,使 __________________________________
F.往容量瓶内加蒸馏水,直到溶液在刻度线下1~2cm处
(4)若出现以下情况,对所配溶液浓度将有何影响?(填“偏高”“偏低”或“无影响”)
定容时俯视刻度线______________,定容后,盖上玻璃塞倒转摇匀,发现液面低于刻度线,继续滴加蒸馏水至刻度线_____。