题目内容
【题目】下表是第三周期部分元素的电离能数据,下列说法正确的是( )
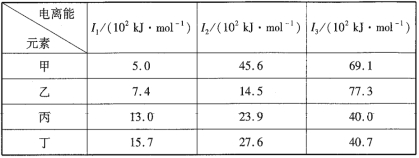
A.甲的金属性比乙弱B.乙的最高正化合价为+1
C.丙一定为非金属元素D.丁一定是金属元素
【答案】C
【解析】
甲、乙、丙、丁为第三周期元素,甲元素的第一电离能远远小于第二电离能,说明A元素最外层有1个电子,失去1个电子时达到稳定结构,所以甲为Na元素;乙元素的第二电离能远远小于第三电离能,则乙元素最外层有2个电子,失去两个电子后达到稳定结构,所以乙为Mg元素;丙、丁元素的第一电离、第二电离能、第三电离能相差不大,说明丙元素最外层电子数大于3,则丙、丁一定为非金属元素。
A. 甲为Na元素,乙为Mg元素,则甲的金属性比乙强,故A错误;
B. 乙为Mg元素,化合价为+2价,故B错误;
C. 丙元素的第一电离、第二电离能、第三电离能相差不大,说明丙元素最外层电子数大于3,则丙一定为非金属元素,故C正确;
D.丁元素的第一电离、第二电离能、第三电离能相差不大,说明丙元素最外层电子数大于3,则丁一定为非金属元素,不可能是金属元素,故D错误;
故选C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】二氧化硫分子(SO2)分子中共有__个σ键,其中心原子(硫原子)的孤电子对数为__;价层电子对数为__,该分子的VSEPR模型为__;则该分子呈__形,二氧化硫分子的中心原子的杂化类型为__。
【题目】某实验小组探究AgNO3溶液与Na2SO3溶液的反应。
实验I | 操作 | 现象 |
| 滴加5滴0.1mol/L Na2SO3溶液,振荡 | 产生白色沉淀,测得混合溶液pH=5 |
继续滴加0.1mol/L Na2SO3溶液,振荡 | 白色沉淀增多,继续滴加,白色沉淀消失,测得混合溶液pH=9 |
资料:Ag2SO3,白色固体,难溶于水;Ag2SO4,白色固体,微溶于水;AgOH,白色固体,常温下不稳定,易分解产生棕褐色固体。
(1)测得0.1mol/L Na2SO3溶液pH=10,用离子方程式解释原因:_______。
(2)实验小组对白色沉淀的成分提出猜想:
①可能含Ag2SO3。
②可能含Ag2SO4,理由是________。
③可能含AgOH。
实验产生的白色沉淀放置一段时间后未发生明显变化,排除猜想③。
(3)检验白色沉淀的成分
(资料:Ag++2S2O32![]() Ag(S2O3)23,Ag(S2O3)23在溶液中稳定存在。)
Ag(S2O3)23,Ag(S2O3)23在溶液中稳定存在。)
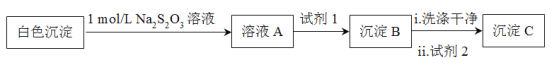
测得沉淀C质量小于沉淀B,试剂1和试剂2分别是_____、______,说明白色沉淀是Ag2SO3和Ag2SO4的混合物。
(4)探究白色沉淀消失的原因。实验小组设计对照实验:
实验II | 实验III | |
实验操作 |
|
|
现象 | 沉淀溶解 |
① 补充实验III的实验操作及现象:_______,证明SO32使白色沉淀溶解。
② 查阅资料:Ag2SO3能溶于过量Na2SO3溶液中形成Ag(SO3)23。白色沉淀中含有g2SO4,但还能全部溶解于Na2SO3溶液的原因是______。
(5)探究AgNO3溶液与Na2SO3溶液能否发生氧化还原反应。
实验IV | 操作 | 现象 |
| 步骤i:滴加一定体积0.1 mol/L Na2SO3溶液 | 产生白色沉淀 |
步骤ii:再加入NaOH溶液调pH=14,振荡 | 白色沉淀变黑,经检验为Ag |
步骤ii中Ag2SO3发生反应的离子方程式是_________。
(6)综合实验I和IV,说明AgNO3溶液与Na2SO3溶液的反应类型与_______有关。