题目内容
【题目】二氧化硫分子(SO2)分子中共有__个σ键,其中心原子(硫原子)的孤电子对数为__;价层电子对数为__,该分子的VSEPR模型为__;则该分子呈__形,二氧化硫分子的中心原子的杂化类型为__。
【答案】2 1 3 平面三角形 V sp2
【解析】
二氧化硫分子(SO2)分子中S和O形成σ键,共有2个σ键,其中心原子(硫原子)的孤电子对数为![]() =1;价层电子对数等于σ键+孤电子对,价层电子对数为2+1=3,该分子的VSEPR模型为平面三角形;孤电子对不占分子形状,则该分子呈V形,根据杂化轨道理论分析,杂化轨道用于成σ键和填充孤电子对,二氧化硫分子的中心原子的杂化类型为sp2。
=1;价层电子对数等于σ键+孤电子对,价层电子对数为2+1=3,该分子的VSEPR模型为平面三角形;孤电子对不占分子形状,则该分子呈V形,根据杂化轨道理论分析,杂化轨道用于成σ键和填充孤电子对,二氧化硫分子的中心原子的杂化类型为sp2。
故答案为: 2 ;1;3 ;平面三角形; V ;sp2。

 阅读快车系列答案
阅读快车系列答案【题目】减少氮的氧化物和碳的氧化物在大气中的排放是环境保护的重要内容之一。合理应用和处理碳、氮及其化合物,在生产生活中有重要意义。
(1)对温室气体 CO2 的研究一直是科技界关注的重点。在催化剂存在下用 H2 还原 CO2 是解决溫室效应的重要手段之一。
已知:①H2 和 CH4 的燃烧热分别为 285.5 kJ/mol 和 890.0 kJ/mol。
②H2O(1)===H2O(g) ΔH=+44 kJ/mol
试写出H2还原CO2生成CH4和H2O(g)的热化学方程式_____。
(2)CO2在CuZnO催化下,可同时发生如下的反应I、II,其可作为解决温室效应及能源短缺的重要手段。
I.CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)ΔH1=-57.8kJ/mol
CH3OH(g)+H2O(g)ΔH1=-57.8kJ/mol
II.CO2(g)+H2(g)![]() CO(g)+H2O(g)ΔH2=+41.2kJ/mol
CO(g)+H2O(g)ΔH2=+41.2kJ/mol
对于气体参加的反应,表示平衡常数Kp时,用气体组分(B)的平衡分压p(B)代替该气体的平衡浓度c(B),则反应II的Kp=_____[已知:气体各组分的分压p(B),等于总压乘以其体积分数]。
在CuZnO存在的条件下,保持温度T不变,在一刚性密闭容器中,充入一定量的CO2及H2,起始及达平衡时,容器内各气体物质的量如下表:
CO2 | H2 | CH3OH | CO | H2O(g) | 总压/kPa | |
起始/mol | 5.0 | 7.0 | 0 | 0 | 0 | p0 |
平衡/mol | n1 | n2 | p |
若反应I、II均达平衡时,p0=1.2p,则表中n1/span>=_____;若此时n2=3.则反应I的平衡常数Kp=_____(无需带单位,用含总压p的式子表示)。
(3)汽车尾气是雾霾形成的原因之一,研究氮氧化物的处理方法可有效减少雾霾的形成。可采用氧化还原法脱硝:4NO(g)+4NH3(g)+O2(g)![]() 4N2(g)+6H2O(g)ΔH<0
4N2(g)+6H2O(g)ΔH<0
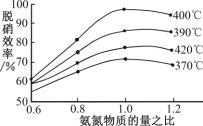
(4)根据图示判断提高脱硝效率的最佳条件是_____;氨氮比一定时,在400℃时,脱硝效率最大,其可能的原因是_____。用活性炭还原法也可以处理氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应:C(s)+2NO(g)![]() N2(g)+CO2(g)ΔH>0在T℃时,反应进行到不同时间测得各物质的量浓度如下:
N2(g)+CO2(g)ΔH>0在T℃时,反应进行到不同时间测得各物质的量浓度如下:
时间/min | 0 | 10 | 20 | 30 | 40 | 50 |
c(NO)/molL1 | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
c(N2)/molL1 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
c(CO2)/molL1 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
30min后,只改变某一条件,根据上表的数据判断改变的条件可能是______填字母)。
A.通入一定量的 CO2 B.加入合适的催化剂 C.适当缩小容器的体积
D.通入一定量的 NO E.加入一定量的活性炭 F.适当升高温度
【题目】盐酸和氢氧化钠是工业上重要的化工原料,也是实验室里常见的化学试剂。欲测定某NaOH溶液的物质的量浓度,可用0.1000 mol·L-1 HCl标准溶液进行中和滴定(用酚酞作指示剂)。请回答下列问题:
(1)滴定时,盛装待测NaOH溶液的仪器名称为_____。
(2)碱式滴定管用蒸馏水洗净后,接下来应该进行的操作是_________。
(3)若甲学生在实验过程中,记录滴定前滴定管内液面读数为0.50 mL,滴定后液面如图,则此时消耗标准溶液的体积为_____。

乙学生做了三组平行实验,数据记录如下:
实验序号 | 待测NaOH溶液的体积/mL | 0.1000mol·L-1HCl溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 0.11 | 25.10 |
2 | 25.00 | 1.56 | 33.30 |
3 | 25.00 | 0.21 | 25.22 |
(4)选取上述合理数据,计算出待测NaOH溶液的物质的量浓度为______(保留四位有效数字)。
(5)下列哪些操作会使测定结果偏高_____ (填序号)。
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后再用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数
(6)滴定达到终点的标志是________。