题目内容
19.NA为阿伏加德罗常数,下列说法正确的是( )| A. | 标准状况下,11.2L的戊烷所含的分子数为0.5NA | |
| B. | 26g乙炔所含共用电子对数目为3NA | |
| C. | 标准状况下,11.2 L CCl4所含分子数为0.5NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA |
分析 A、标况下,戊烷为液体;
B、求出乙炔的物质的量,然后根据1mol乙炔中含5mol共用电子对来分析;
C、标况下,四氯化碳为液体;
D、乙烯、丙烯和丁烯的最简式均为CH2.
解答 解:A、标况下,戊烷为液体,故不能根据气体摩尔体积来计算其物质的量,故A错误;
B、26g乙炔的物质的量为1mol,而1mol乙炔中含5mol共用电子对,即5NA个,故B错误;
C、标况下,四氯化碳为液体,故不能根据气体摩尔体积来计算其物质的量,故C错误;
D、乙烯、丙烯和丁烯的最简式均为CH2,故14g混合物中含有的CH2的物质的量为1mol,故含有3mol原子即3NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,注意掌握公式的运用和物质的结构,难度不大.

练习册系列答案
相关题目
7.下列关于反应能量的说法正确的是( )
| A. | Zn(s)+CuSO4(aq)═ZnSO4(aq)+Cu(s)△H=-216kJ•mol-1,则反应物总能量>生成物总能量 | |
| B. | 相同条件下,如果1mol氢原子所具有的能量为E1,1mol 氢分子所具有的能量为E2,则2E1=E2 | |
| C. | 101 kPa时,2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1,则H2的燃烧热为△H=-571.6 kJ•mol-1 | |
| D. | H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,则1molNaOH的氢氧化钠固体与含0.5molH2SO4的稀硫酸混合后放出57.3kJ的热量 |
14.下列电子式正确的是( )
| A. | 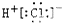 | B. | 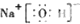 | C. | 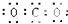 | D. | 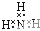 |
4.某组成为C3H5O2C1的纯净有机物A与Na0H水溶液共热,产物酸化后可得到分子组成为C3H6O3的有机物B,在适当条件下,每两分子的B可相互发生酯化反应,生成1分子C,那么C的结构不可能是( )
| A. | CH3CH(OH)C00CH(CH3)C00H | B. | CH3CH(OH)C00CH2CH2C00H | ||
| C. | 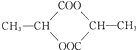 | D. | 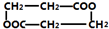 |
11.下列关于物质性质变化的比较,不正确的是( )
| A. | 酸性:HI>HBr>HCl>HF | B. | 沸点:HI>HBr>HCl>HF | ||
| C. | 还原性:HI>HBr>HCl>HF | D. | 热稳定:HF>HCl>HBr>HI |
8.NA代表阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 1mol的羟基与1mol的氢氧根离子所含电子数均为9NA | |
| B. | 120g NaHSO4固体中含有的离子总数为3NA | |
| C. | 1mol Na被氧化生成Na2O2或NaCl,都失去NA个电子 | |
| D. | 1.0L 1.0mol•L-1的NaNO3水溶液中含有的氧原子数为3NA |
 根据要求回答下列问题:
根据要求回答下列问题: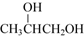 +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$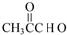 +2H2O.
+2H2O.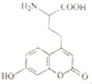 1molNaOH溶液反应最多消耗4molNaOH,1mol该物质因发生加成反应可消耗1molBr2.
1molNaOH溶液反应最多消耗4molNaOH,1mol该物质因发生加成反应可消耗1molBr2.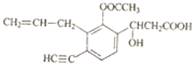 该分子中一定与苯环处于同一平面的碳原子有4个(不包括苯环上的碳原子),分子中含有2种双键.
该分子中一定与苯环处于同一平面的碳原子有4个(不包括苯环上的碳原子),分子中含有2种双键.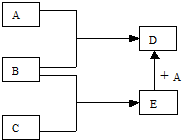 已知A、B、C、D、E均为常见物质,在一定条件下相互转化关系如图所示(反应条件和部分产物已省略).
已知A、B、C、D、E均为常见物质,在一定条件下相互转化关系如图所示(反应条件和部分产物已省略).