题目内容
7.下列关于反应能量的说法正确的是( )| A. | Zn(s)+CuSO4(aq)═ZnSO4(aq)+Cu(s)△H=-216kJ•mol-1,则反应物总能量>生成物总能量 | |
| B. | 相同条件下,如果1mol氢原子所具有的能量为E1,1mol 氢分子所具有的能量为E2,则2E1=E2 | |
| C. | 101 kPa时,2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1,则H2的燃烧热为△H=-571.6 kJ•mol-1 | |
| D. | H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,则1molNaOH的氢氧化钠固体与含0.5molH2SO4的稀硫酸混合后放出57.3kJ的热量 |
分析 A、当反应物总能量>生成物总能量,则反应是放热反应;
B、物质的能量越低越稳定,形成化学键过程是放热过程;
C、燃烧热必须是1mol物质燃烧生成最稳定的氧合物所放出的能量;
D、中和热是强酸和强碱发生中和反应生成1mol水时,所放出的热量.
解答 解:A、当反应物总能量>生成物总能量,则反应是放热反应,△H<O,故A正确;
B、如果1mol氢原子所具有的能量为E1,1mol氢分子的能量为E2.原子的能量比分子的能量高,所以原子灰结合成分子形成化学键放出热量,即2H=H2 放出热量,则2E1>E2,故B错误;
C、H2的燃烧热必须是1mol物质燃烧生成最稳定的氧合物液态水时所放出的能量,故C错误;
D、中和热是强酸和强碱的稀溶液发生中和反应生成1mol水时,所放出的热量,1molNaOH的氢氧化钠固体与含0.5molH2SO4的稀硫酸混合时,氢氧化钠固体溶于水放热,所以导致△H<-57.3kJ•mol-1,故D错误.
故选A.
点评 本题考查化学反应中的能量变化的有关知识,主要是反应的能量守恒的应用,形成化学键是放热反应,燃烧热、中和热的概念应用,可以根据所学知识进行回答,难度不大.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
17.T℃时,在容积恒定的密闭容器中A气体与B气体反应生成C气体,反应过程中A、B、C浓度的变化如图a所示,若保持其他条件不变,温度分别为T1和T2时,B的体积百分含量与时间的关系如图b所示,则下列结论正确的是
( )
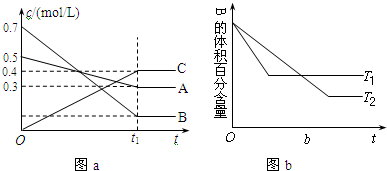
( )

| A. | 其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大 | |
| B. | T℃时,若在该容器中由0.4mol/LA、0.4mol/LB和0.2mol/LC反应,达到平衡后,C的浓度仍为0.4mol/L | |
| C. | 在(t1+10)min时,保持其他条件不变,增大压强,平衡向逆反应方向移动 | |
| D. | (t1+10)min时,保持压强不变,通入稀有气体,平衡向正反应方向移动 |
18.由物质的分类知识可知,下列生活中常见的物质属于同一类的是( )
| A. | 铝合金、钢 | B. | 加碘食盐、纯碱 | C. | 冰水、冰镇汽水 | D. | 氧气、空气 |
12.下列物质中最简式相同,但既不是同系物,也不是同分异构体,又不含相同官能团的是( )
| A. | CH3CH=CH2和  | B. | 乙炔和苯 | C. | 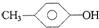 和 和  | D. | 甲醛和甲酸甲酯 |
19.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,11.2L的戊烷所含的分子数为0.5NA | |
| B. | 26g乙炔所含共用电子对数目为3NA | |
| C. | 标准状况下,11.2 L CCl4所含分子数为0.5NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA |
16.某种烷烃11g完全燃烧时,需要28L氧气(标准状况下),该烷烃是( )
| A. | C5Hl2 | B. | C4H10 | C. | C3H8 | D. | C2H6 |
17.能说明苯分子中没有单双键存在,且分子为平面正六边形结构的依据是( )
| A. | 苯分子的核磁共振图表明分子中只存在一种氢原子 | |
| B. | 邻二甲苯没有同分异构体 | |
| C. | 间二甲苯没有同分异构体 | |
| D. | 对二甲苯没有同分异构体 |
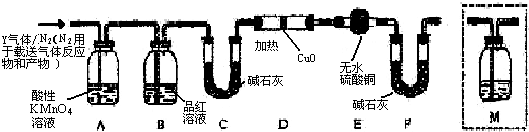
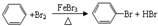 ,预测该芳香烃能(填“能”或“不能”)发生该类反应.
,预测该芳香烃能(填“能”或“不能”)发生该类反应. b.
b.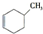 c.
c.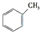
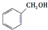 c.
c.
