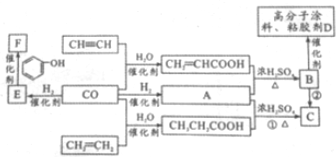
题目内容
11.化学与科学、社会、技术和环境密切相关.下列有关说法中错误的是( )| A. | 目前科学家已制得单原子层锗,其电子迁移率是硅的10倍,有望用于制造高能计算机芯片 | |
| B. | 2014年在西非国家爆发了埃博拉疫情,埃博拉病毒对化学药品敏感,乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的 | |
| C. | 2014年德美科学家因开发超分辨荧光显微镜获诺贝尔化学奖,使光学显微镜分辨率步入了纳米时代,利用此类光显微镜可以观察活细胞内蛋白质等大分子 | |
| D. | 绿色化学期望利用化学原理从源头消除污染,在生产过程中充分利用原料,实现零排放 |
分析 A.制造高能计算机芯片的晶体管应为半导体材料;
B.乙醇为有机物能够使蛋白质变性;
C.依据2014年诺贝尔化学奖获得者及其贡献解答;
D.根据绿色化学的内涵和外延知识来回答判断.
解答 解;A.晶体管材料应具有导电性,锗电子迁移率比硅强,为良好的半导体材料,故A正确;
B.乙醇消毒液消毒是因为可以使蛋白质变性,而并非是将病毒氧化,故B错误;
C.2014年德美科学家因开发超分辨率荧光显微镜获诺贝尔化学奖,使光学显微镜分辨率步入了纳米时代.利用此类光学显微镜可以观察活细胞内蛋白质等大分子,故C正确;
D.依据绿色化学的含义可知,绿色化学是利用化学原理从源头消除污染,在化学过程中充分利用原料,实现零排放,故D正确;
故选:B.
点评 本题为综合题,考查了化学史、物质的性质和用途、绿色化学的概念,依据相关知识即可解答,注意对基础知识的积累.

练习册系列答案
相关题目
2.相同温度下,容积均恒为2L的甲、乙、丙3个密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g)△H=-197kJ•mol-l.实验测得起始、平衡时的有关数据如下表:下列叙述正确的是( )
| 容器 | 起始各物质的物质的量/mol | 达到平衡时体系能量的变化 | |||
| SO2 | O2 | SO3 | Ar | ||
| 甲 | 2 | 1 | 0 | 0 | 放出热量:Q1 |
| 乙 | 1.8 | 0.9 | 0.2 | 0 | 放出热量:Q2=78.8kJ |
| 丙 | 1.8 | 0.9 | 0.2 | 0.1 | 放出热量:Q3 |
| A. | Q1>Q3>Q2=78.8kJ | |
| B. | 三个容器中反应的平衡常数均为K=2 | |
| C. | 甲中反应达到平衡时,若升高温度,则SO2的转化率将大于50% | |
| D. | 若乙容器中的反应经tmin达到平衡,则0~tmin内,v(O2)=$\frac{1}{5t}$ mol/(L•min) |
19.短周期元素X、Y、Z、W,它们的原子序数依次增大.X与Z同主族,且原子序数之和为20.Y原子的质子数为Z原子的质子数的一半,W原子的最外层电子数比Y原子的最外层电子数多2个.下列叙述正确的是( )
| A. | 原子半径Z>W>Y>X | |
| B. | 气态氢化物的稳定性Z>W | |
| C. | Y的最高价氧化物对应的水化物可与其气态氢化物发生化合反应 | |
| D. | X的气态氢化物与足量W单质在光照条件下反应所得生成物均为气体 |
6.下列物质中同分异构体数目最多的是( )
| A. | C2H6O | B. | C3H8O | C. | C3H6BrCl | D. | C4H9Cl |
3.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1mol Na2O和Na2O2的混合物中,阴阳离子总数为3NA | |
| B. | 非标准状况下,NA个CO2分子所占的条件不可能为22.4L | |
| C. | 24.4gNa2O•SiO2中含有0.2NA个SiO2分子 | |
| D. | 56gFe投入1000mL3.5mol•L-1稀硝酸中,充分反应,转移电子总数为3NA |
20.铝是我们很熟悉的一种金属元素,铊(Tl)和铝均位于元素周期表中的第ⅢA族,铊属于第三周期.则关于铊的下列性质中判断错误的是( )
| A. | 是银白色质软的金属 | B. | 能形成+3价的化合物 | ||
| C. | Tl(OH)3一定是两性氢氧化物 | D. | 单质铊的还原性一定比单质铝强 |
1.分析下列各项结构的规律,按此规律排布第10项的分子式应为( )
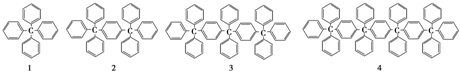

| A. | C198H146 | B. | C196H155 | C. | C196H146 | D. | C198H155 |