题目内容
17.2003年4月重庆市天原化工总厂发生了严重的氯气汇漏和爆炸事故,在此次事故中有9人死亡,3人受伤,15万人紧急疏散.根据你所学知识回答下列问题:(1)氯气为黄绿色气体,有强烈的刺激性气味,氯气发生泄漏后政府立即组织周围的群众紧急疏散,这是由于氯气有毒
(2)事故发生后消防官兵迅速赶到现场,不断地向漏气罐周围喷射水幕,这样做的目的是氯能溶于水,从而减少氯气散失;此外他们还采用了用铁管将末泄漏的氯气引到附近的嘉陵江边的水池中,同时注入碱水,这样做的目的是2OH-+Cl2=Cl-+ClO-+H2O(用离子方程式表示).
分析 (1)根据不需要通过化学变化表现出来的性质为物质的物理性质的概念,找出物质的颜色、状态、味道、密度、溶解性等方面的性质;
(2)氯能溶于水,氯气与碱反应生成盐和水.
解答 解:(1)题中描述到氯气的物理性质有:在常温下,氯气为黄绿色气体,有刺激性气味,能溶于水,密度为3.21g/L,氯气有毒,故答案为:刺激性;有毒;
(2)不断地向漏气罐周围喷射水幕,氯能溶于水,从而减少氯气散失,注入碱水,这样做的目的是氯气与碱反应生成盐和水,反应的离子方程式为:2OH-+Cl2=Cl-+ClO-+H2O,故答案为:氯能溶于水,从而减少氯气散失;2OH-+Cl2=Cl-+ClO-+H2O.
点评 本题主要考查物质的性质和离子方程式的书写等方面的知识,书写离子方程式时要注意遵循质量守恒定律和电荷守恒.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
7.X、Y、Z、W是元素周期表前四周期中常见的元素,其相关信息如表:
(1)Z位于元素周期表第三周期第IA族,其原子有11个电子.
(2)X单质的氧化性比Y单质的氧化性小(填“大”或“小”);X 最高价氧化物的电子式为: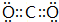 .
.
(3)写出含Z,Y两种元素的淡黄色化合物与XY2反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2.
(4)与Z位于同周期且半径最小的金属元素的最高价氧化物的水化物能与Z的最高价氧化物的水化物反应,该反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O.
| 元素 | 相关信息 |
| X | X原子的L层电子数是K层电子数的2倍 |
| Y | Y的原子最外层电子数为层数的3倍 |
| Z | Z存在质量数为23,中子数为12的核素 |
| W | W有多种化合价,其白色化合物在空气中会迅速变成灰绿色,最后变成红褐色 |
(2)X单质的氧化性比Y单质的氧化性小(填“大”或“小”);X 最高价氧化物的电子式为:
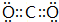 .
.(3)写出含Z,Y两种元素的淡黄色化合物与XY2反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2.
(4)与Z位于同周期且半径最小的金属元素的最高价氧化物的水化物能与Z的最高价氧化物的水化物反应,该反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O.
12.常温下,下列各组离子一定能在指定溶液中大量共存的是( )
| A. | pH=13 的溶液:Na+、NH4+、SO42-、Cl- | |
| B. | 甲基橙呈黄色的溶液:Na+、K+、ClO-、AlO2- | |
| C. | 0.1 mol/L 的KNO3 溶液:H+、Fe2+、Cl-、SO42- | |
| D. | 水电离的c(H+)=1×10-13mol.L-1的溶液中:K+、Ba2+、Br-、I- |
2.下列溶液中,需要避光保存的是( )
①氯水 ②浓盐酸 ③硝酸 ④浓硫酸.
①氯水 ②浓盐酸 ③硝酸 ④浓硫酸.
| A. | ① | B. | ①②③④ | C. | ①③ | D. | ②③ |
20.常温下,现有0.1mol/L的NH4HCO3溶液,pH=7.8.已知含氮(或含碳)各微粒的分布分数(平衡时某种微粒的浓度占各种微粒浓度之和的分数)与pH的关系如图所示.下列说法正确的是( )

| A. | 当溶液的pH=9时,溶液中存在下列关系:c(NH4+)>c(HCO3-)>c(NH3•H2O)>c(CO32-) | |
| B. | NH4HCO3溶液中存在下列守恒关系:c(NH4+)+c(NH3•H2O)+c(H+)=c(OH-)+2c(CO32-)+c(H2CO3) | |
| C. | 往该溶液中逐滴滴加氢氧化钠时NH4+和HCO3-浓度逐渐减小 | |
| D. | 通过分析可知常温下Kb(NH3•H2O)>Ka1(H2CO3) |