题目内容
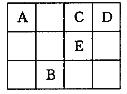
【题目】下表为元素周期表的一部分,其中A、C、D、E为短周期元素,最外层电子数之和为23,下列说法正确的是
A.元素A的氢化物,在同族元素中沸点最低
B.元素B的金属性比E弱
C.A、C、D均可形成18e-分子
D.与金属钠的反应中,1mol C原子和1 mol E原子得电子数目一定相等
【答案】C
【解析】
下表为元素周期表的一部分,其中A、C、D、E为短周期元素,最外层电子数之和为23,A、C、D位于第二周期,E位于第三周期,B位于第四周期;设C、E的最外层电子数为x,A、D最外层电子数分别为x-2、x+1,则2x+x-2+x+1=23,解得x=6,所以A为C元素,B为As元素,C为O,E为S,D为Cl元素,据此解答。
A.由A为C元素,元素A的氢化物为CH4,根据组成和结构相同的同主族氢化物的沸点随着相对原子质量增加而升高,所以CH4在同族元素氢化物中沸点最低,故A正确;
B.由B为As元素,E为S,均为非金属,且S的非金属性比As弱,故B错误;
C.由A为C元素,C为O,D为Cl元素,他们能形成的18e-分子分别为乙烷、双氧水和HCI,故C正确;
D.与金属钠的反应生成过氧化钠中O的化合价为-1,生成的硫化钠中S的化合价为-2,则1molO原子和1molS原子得电子数目不相等,故D错误;
故选:C。

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目