��Ŀ����
����������ͨ����˵�ġ���������������ᡱ��ָ���ᡢ��������ᣬ�������ָ�ռ�ʹ��
��1�������ʷ���ĽǶȷ���������˵���в�ǡ����һ�������� ���ѧʽ����
��2���������м���ŨH2SO4ʱ�����а������ɣ��������������ڵ��²����������ԭ���� ��
A��ŨH2SO4������ˮ�� B��ŨH2SO4������ˮ��
C��������лӷ��� D���������ʵ��ܽ�����¶����߶�����
��3������ѧ��ѧ���������ʵ�����Ʒ��У�����Ũ�����Ʊ�������Ļ�ѧʽ�� ���������֣�
��4���١����ᡱ�������ܽ�����ͽ�����������п�״�����ڳ������ܹ�ȫ������������Ũ������� ��
A��Au B��Ag C��Al D��Fe
�ڽ���ͭͶ��ϡ�����в�������Ӧ�����ټ���H2O2��Һ��ͭ��ʼ�ܽ⣬��Һ��Ϊ��ɫ�������÷�Ӧ���Ϊԭ��أ�������ӦʽΪ�� ��
��5���ռ������Һ��������CO2���壮����0.1mol NaOH����Һ����һ����CO2����Һ����С�����ɣ��Ƶù�������Ϊ8�ˣ������õ��Ĺ��������ܽ���ˮ�������м���1mol/L������120mL����ַ�Ӧ���ٽ���Һ���ɣ����յõ����������Ϊ g��
��1�������ʷ���ĽǶȷ���������˵���в�ǡ����һ��������
��2���������м���ŨH2SO4ʱ�����а������ɣ��������������ڵ��²����������ԭ����
A��ŨH2SO4������ˮ�� B��ŨH2SO4������ˮ��
C��������лӷ��� D���������ʵ��ܽ�����¶����߶�����
��3������ѧ��ѧ���������ʵ�����Ʒ��У�����Ũ�����Ʊ�������Ļ�ѧʽ��
��4���١����ᡱ�������ܽ�����ͽ�����������п�״�����ڳ������ܹ�ȫ������������Ũ�������
A��Au B��Ag C��Al D��Fe
�ڽ���ͭͶ��ϡ�����в�������Ӧ�����ټ���H2O2��Һ��ͭ��ʼ�ܽ⣬��Һ��Ϊ��ɫ�������÷�Ӧ���Ϊԭ��أ�������ӦʽΪ��
��5���ռ������Һ��������CO2���壮����0.1mol NaOH����Һ����һ����CO2����Һ����С�����ɣ��Ƶù�������Ϊ8�ˣ������õ��Ĺ��������ܽ���ˮ�������м���1mol/L������120mL����ַ�Ӧ���ٽ���Һ���ɣ����յõ����������Ϊ
���㣺�ᡢ��Ρ�������ĸ�������ϵ,��ѧ����ʽ���йؼ���,����Ļ�ѧ����,Ũ���������
ר�⣺Ԫ�ؼ��仯����
��������1����������εĸ����������ɷ����жϣ��������Σ�
��2���������Ũ������Һ�¶����ߣ������Ȼ����ܽ�ȼ�С���ӷ�����������ˮ�����γ�����СҺ�η����жϣ�
��3������ʵ���������Ʊ�ԭ�����������������Ȼ��⡢�����⡢��ϩ�����嶼������Ũ����������Ʊ���
��4���ٽ�����Ũ���ᷴӦʱ�����������������ۻ�������ֹ��Ӧ���У��𡢲�����Ũ���ᷴӦ��
�ڹ���������������Һ�о��������ԣ�
��5����0.1mol NaOH����Һ����һ����CO2����2NaOH+CO2=Na2CO3+H2O��NaOH+CO2=NaHCO3���õ��Ĺ��������ܽ���ˮ�������м������ᣬ���������������ʵ����������ʵ�������������ΪNaCl�������ԭ���غ���㣮
��2���������Ũ������Һ�¶����ߣ������Ȼ����ܽ�ȼ�С���ӷ�����������ˮ�����γ�����СҺ�η����жϣ�
��3������ʵ���������Ʊ�ԭ�����������������Ȼ��⡢�����⡢��ϩ�����嶼������Ũ����������Ʊ���
��4���ٽ�����Ũ���ᷴӦʱ�����������������ۻ�������ֹ��Ӧ���У��𡢲�����Ũ���ᷴӦ��
�ڹ���������������Һ�о��������ԣ�
��5����0.1mol NaOH����Һ����һ����CO2����2NaOH+CO2=Na2CO3+H2O��NaOH+CO2=NaHCO3���õ��Ĺ��������ܽ���ˮ�������м������ᣬ���������������ʵ����������ʵ�������������ΪNaCl�������ԭ���غ���㣮
���
�⣺��1����Ϊ�������������ȫ�������������ӵĻ�����������Ҫ�ɷ���Na2CO3��̼���Ƶ���������Ӻ�̼������ӣ������Σ�
�ʴ�Ϊ��Na2CO3��
��2���������м���ŨH2SO4ʱ�����а������ɣ�����ΪŨ�����ܽ�����з���ʹ��Һ�¶����ߣ��Ȼ���ӷ��ڿ���������ˮ�����γ�����СҺ�Σ�
A��ŨH2SO4������ˮ�Բ��Dz��������ԭ��Aѡ��
B��Ũ���������ˮ�ԣ��ܽ�����з��ȣ��������ʵ��ܽ�����¶����߶����ͣ��Ȼ���ӷ�����B��ѡ��
C������������Ϊ������лӷ��ԣ��ӷ������Ȼ����γɣ���C��ѡ��
D��Ũ��������ˮ�ɷų��������ȣ��Ȼ���ӷ��ڿ���������ˮ�����γ�����СҺ�Σ���D��ѡ��
��ѡ��A��
��3��������������Ũ������������Ʒ�Ӧ���ɣ��Ȼ������ù����Ȼ��ƺ�Ũ������ȷ�Ӧ���ɣ������������÷����ƺ�Ũ���ᷴӦ�Ƶã���ϩ�������Ҵ���Ũ������ȷ�Ӧ�Ʊ���
�ʴ�Ϊ��SO2��C2H4 ����HCl��HF����
��4���ٽ����ڳ������ܹ�ȫ������������Ũ�������������Ӧ�������������·����ۻ�����Ӧ���ټ�������ѡ��B��
�ڽ���ͭͶ��ϡ�����в�������Ӧ�����ټ���H2O2��Һ��ͭ��ʼ�ܽ⣬��Һ��Ϊ��ɫ��˵������������������Һ�о����������ܽ�ͭ�����ӷ���ʽΪ��Cu+H2O2+2H+=Cu2++2H2O�������÷�Ӧ���Ϊԭ��أ�������ӦʽΪΪ��������õ���������ˮ���缫��ӦΪ��H2O2+2H++2e-=2H2O��
�ʴ�Ϊ��H2O2+2H++2e-=2H2O��
��5����0.1mol NaOH����Һ����һ����CO2����2NaOH+CO2=Na2CO3+H2O��NaOH+CO2=NaHCO3�������ߵ����ʵ����ȴ���2��1��������̼���㣬��С�����ɵõ�����ΪNa2CO3��NaOH������2��1ʱ����ΪNa2CO3��1��1ʱ����ΪNaHCO3������2��2��2��1֮��ʱ����ΪNa2CO3��NaHCO3������̼������������Ԫ���غ�����֪����=0.1mol��
��106g/mol=5.3g����Ϊ̼����������=0.1g��84g/mol=8.4g������Һ����С�����ɣ��Ƶù�������Ϊ8�ˣ�˵������Ϊ̼���ƺ�̼�����ƻ��������õ��Ĺ��������ܽ���ˮ�������м���1mol/L������120mL�����ܽ����̼���ƣ���Ҫ�Ȼ���0.1mol�����ܽ����̼�����ƣ���Ҫ�Ȼ������ʵ���Ϊ0.1��mol��˵�������������ַ�Ӧ���ٽ���Һ���ɣ��õ����ʹ���NaCl��������ԭ���غ����õ���������=0.1mol��58.5g/mol=5.85g��
�ʴ�Ϊ��5.85��
�ʴ�Ϊ��Na2CO3��
��2���������м���ŨH2SO4ʱ�����а������ɣ�����ΪŨ�����ܽ�����з���ʹ��Һ�¶����ߣ��Ȼ���ӷ��ڿ���������ˮ�����γ�����СҺ�Σ�
A��ŨH2SO4������ˮ�Բ��Dz��������ԭ��Aѡ��
B��Ũ���������ˮ�ԣ��ܽ�����з��ȣ��������ʵ��ܽ�����¶����߶����ͣ��Ȼ���ӷ�����B��ѡ��
C������������Ϊ������лӷ��ԣ��ӷ������Ȼ����γɣ���C��ѡ��
D��Ũ��������ˮ�ɷų��������ȣ��Ȼ���ӷ��ڿ���������ˮ�����γ�����СҺ�Σ���D��ѡ��
��ѡ��A��
��3��������������Ũ������������Ʒ�Ӧ���ɣ��Ȼ������ù����Ȼ��ƺ�Ũ������ȷ�Ӧ���ɣ������������÷����ƺ�Ũ���ᷴӦ�Ƶã���ϩ�������Ҵ���Ũ������ȷ�Ӧ�Ʊ���
�ʴ�Ϊ��SO2��C2H4 ����HCl��HF����
��4���ٽ����ڳ������ܹ�ȫ������������Ũ�������������Ӧ�������������·����ۻ�����Ӧ���ټ�������ѡ��B��
�ڽ���ͭͶ��ϡ�����в�������Ӧ�����ټ���H2O2��Һ��ͭ��ʼ�ܽ⣬��Һ��Ϊ��ɫ��˵������������������Һ�о����������ܽ�ͭ�����ӷ���ʽΪ��Cu+H2O2+2H+=Cu2++2H2O�������÷�Ӧ���Ϊԭ��أ�������ӦʽΪΪ��������õ���������ˮ���缫��ӦΪ��H2O2+2H++2e-=2H2O��
�ʴ�Ϊ��H2O2+2H++2e-=2H2O��
��5����0.1mol NaOH����Һ����һ����CO2����2NaOH+CO2=Na2CO3+H2O��NaOH+CO2=NaHCO3�������ߵ����ʵ����ȴ���2��1��������̼���㣬��С�����ɵõ�����ΪNa2CO3��NaOH������2��1ʱ����ΪNa2CO3��1��1ʱ����ΪNaHCO3������2��2��2��1֮��ʱ����ΪNa2CO3��NaHCO3������̼������������Ԫ���غ�����֪����=0.1mol��
| 1 |
| 2 |
�ʴ�Ϊ��5.85��
���������⿼���˻�ѧ��Ӧ����������������ʵ�Ӧ�ã�ע�������̼������������Һ��Ӧ������жϼ���Ӧ�ã����ջ����ǹؼ�����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
�����£���20mL 0.1mol?L-1 NaOH��Һ��V mL 0.1mol?L-1 HX��Һ�����кͷ�Ӧ���õ������ҺpH=a�������й�˵����ȷ���ǣ�������
| A����a��7����һ����V��20 |
| B����a=7����һ����c��Na+��=c��X-�� |
| C����V��20����һ����c��Na+����c��X-����c��OH-����c��H+�� |
| D����V=20����һ����c��Na+��+c��H+��=c��HX��+c��X-��+c��OH+�� |
��60g�ɼ������ϩ��ɵĻ������ͨ��ʢ��������ˮ�������ʢ��ˮ������������������28g����ԭ������м������ϩ�����ʵ���֮��Ϊ��������
| A��1��2 | B��2��1 |
| C��3��2 | D��2��3 |
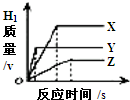 ����ͬ�������ͬ���������̵ֽ�ϡ���ᣬ�ֱ���뵽��������������С��ͬ��X��Y��Z���ֽϻ��ý����У�������ȫ��Ӧ��������H2�������뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ������˵������ȷ���ǣ�������
����ͬ�������ͬ���������̵ֽ�ϡ���ᣬ�ֱ���뵽��������������С��ͬ��X��Y��Z���ֽϻ��ý����У�������ȫ��Ӧ��������H2�������뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ������˵������ȷ���ǣ�������| A�����ֽ����Ļ��˳��ΪY��X��Z |
| B����������������˳��ΪX��Y��Z |
| C������ϡ���������˳��ΪZ��Y��X |
| D�����ԭ�������ɴ�С��˳��ΪX��Y��Z |
��NA��ʾ�����ӵ�������ֵ������˵����ȷ���ǣ�������
| A����״���£�0.1mol Cl2����ˮ��ת�Ƶĵ�����ĿΪ0.1NA |
| B�����³�ѹ�£�18g H2O�к��е�ԭ������Ϊ3NA |
| C����״���£�11.2L HF�к��еķ�����ĿΪ0.5NA |
| D�����³�ѹ�£�2.24L CO��CO2��������к��е�̼ԭ����ĿΪ0.1NA |
�������ڻ�ѧ���ʵ��� ��������
| A���ܽ��� | B���ӷ��� |
| C��������� | D�������� |
 ��֪��N2O4��g��?2NO2��g����H=+57.20kJ?mol-1��
��֪��N2O4��g��?2NO2��g����H=+57.20kJ?mol-1��