题目内容
下表列出了除去物质中所含少量杂质的方法,其中错误的是( )
| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | CO | CO2 | 通过足量氢氧化钠溶液,干燥 |
| B | NaCl | 泥沙 | 溶解、过滤、蒸发 |
| C | NaOH溶液 | Na2CO3 | 加入足量稀盐酸至不再产生气泡 |
| D | Cu(NO3)2溶液 | AgNO3 | 加入过量的铜粉,过滤 |
| A、A | B、B | C、C | D、D |
考点:物质的分离、提纯的基本方法选择与应用,物质的分离、提纯和除杂
专题:化学实验基本操作
分析:A.二氧化碳与NaOH反应,而CO不能;
B.泥沙不溶于水,NaCl溶于水;
C.二者均与HCl反应;
D.Cu与硝酸银反应生成硝酸铜.
B.泥沙不溶于水,NaCl溶于水;
C.二者均与HCl反应;
D.Cu与硝酸银反应生成硝酸铜.
解答:
解:A.二氧化碳与NaOH反应,而CO不能,则通过足量氢氧化钠溶液,干燥可除杂,故A正确;
B.泥沙不溶于水,NaCl溶于水,则溶解、过滤、蒸发可分离,故B正确;
C.二者均与HCl反应,不能除杂,应加适量的氢氧化钙溶液过滤来除杂,故C错误;
D.Cu与硝酸银反应生成硝酸铜,则加入过量的铜粉,过滤可除杂,故D正确;
故选C.
B.泥沙不溶于水,NaCl溶于水,则溶解、过滤、蒸发可分离,故B正确;
C.二者均与HCl反应,不能除杂,应加适量的氢氧化钙溶液过滤来除杂,故C错误;
D.Cu与硝酸银反应生成硝酸铜,则加入过量的铜粉,过滤可除杂,故D正确;
故选C.
点评:本题考查混合物分离、提纯方法及选择,为高频考点,把握物质的性质及性质差异为解答的关键,注意除杂的原则和分离方法,题目难度不大.

练习册系列答案
相关题目
(双项)下列说法正确的是( )
| A、氢键是一种化学键 |
| B、氢键使物质具有较高的熔、沸点 |
| C、能与水分子形成氢键的物质易溶于水 |
| D、水结成冰体积膨胀与氢键无关 |
下列关于碳酸钠和碳酸氢钠的比较中,正确的是( )
| A、二者在水中的溶解度不同,碳酸氢钠的溶解度大于碳酸钠的溶解度 |
| B、二者热稳定性不同,碳酸钠的热稳定性大于碳酸氢钠的热稳定性 |
| C、二者都能与盐酸反应放出二氧化碳气体,但产气量和反应快慢不同 |
| D、二者在一定的条件下可以相互转化 |
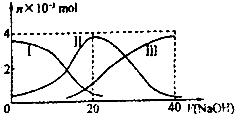 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量 变化如图(其中I代表H2A,Ⅱ代表HA-,Ⅲ代表A2-).根据图示判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量 变化如图(其中I代表H2A,Ⅱ代表HA-,Ⅲ代表A2-).根据图示判断,下列说法正确的是( )| A、当V(NaOH)=20mL时,溶液中离子浓度大小关系 c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
| B、等体积等浓度的NaOH溶液与H2A溶液混合后其溶液中水的电离程度比纯水大 |
| C、欲使NaHA溶液呈中性,可以向其中加入酸或碱 |
| D、向NaHA溶液加人水的过程中,pH可能增大也可能减小 |
已知在2L密闭容器内,发生:2NO(g)+O2(g)?2NO2(g),不能说明该反应已达到平衡状态的是( )
| A、容器内颜色保持不变 |
| B、v逆(NO)═2v正(O2) |
| C、单位时间内生成a mol的O2,同时生成2a mol NO2 |
| D、容器内密度保持不变 |
X元素的阳离子和Y元素的阴离子具有相同的核外电子层结构.下列叙述中正确的是( )
| A、原子序数:X<Y |
| B、原子半径:X<Y |
| C、原子半径:X>Y |
| D、原子最外层电子数:X<Y |
草酸是二元中强酸,草酸氢钠溶液显酸性.常温下,向10mL 0.01mol?L-1 NaHC2O4溶液中滴加0.01mol?L-1 NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是( )
| A、V(NaOH)=0时,c(H+)=1×10-2mol?L-1 |
| B、V(NaOH)<10mL时,可能存在c(Na+)=2c(C2O42-)+c(HC2O4-) |
| C、V(NaOH)=10mL时,c(H+)=1×10-7mol/L |
| D、V(NaOH)>10mL时,一定有c(Na+)>c(C2O42-)>c(OH-)>c(HC2O4-) |
下列实验中,不能观察到明显现象的是( )
| A、把一段打磨过的铝条放入少量冷水中 |
| B、把氯气通入到FeSO4溶液中 |
| C、把绿豆大的钾投入乙醇中 |
| D、把溴水滴加到KI淀粉溶液中 |