题目内容
将60g由甲烷和乙烯组成的混合气体通入盛有足量溴水的容器里,盛溴水的容器的总质量增加28g,则原混合气中甲烷和乙烯的物质的量之比为( )
| A、1:2 | B、2:1 |
| C、3:2 | D、2:3 |
考点:乙烯的化学性质,化学方程式的有关计算
专题:有机物的化学性质及推断
分析:甲烷与溴水不反应,乙烯含有碳碳双键能与溴发生加成反应,依据溴水的质量增加量计算出乙烯的质量和物质的量,然后依据混合气体的质量为60g,计算甲烷的质量和物质的量.
解答:
解:甲烷为饱和烷烃性质稳定,与溴水不反应,乙烯与溴水发生加成反应,所以溴水增加的质量就是乙烯的质量,所以n(C2H4)=
=1mol,所以甲烷的质量为:60g-28g=32g,n(CH4)=
=2mol,则n(CH4):n(C2H4)=2:1,
故选:B.
| 28g |
| 28g/mol |
| 32g |
| 16g/mol |
故选:B.
点评:本题考查了乙烯的性质,题目难度不大,明确乙烯为不饱和烃、甲烷为饱和烃的结构特点是解题关键,注意对基础知识的记忆.

练习册系列答案
相关题目
如图是元素周期表的一部分,有关说法不正确的是( )
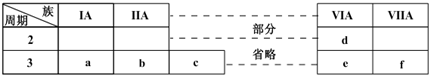

| A、b、d、f四种元素的原子半径:b>f>d |
| B、元素b的单质不能与酸性氧化物发生化学反应 |
| C、元素c的氧化物既能与酸反应,又能与碱反应 |
| D、a、c、e的最高价氧化物对应的水化物之间能够相互反应 |
下列实验能达到目的是( )
| A、用浓HNO3与Cu反应制备NO2 |
| B、用BaCl2溶液鉴别CO2与SO2 |
| C、用溴水鉴别苯和正已烷 |
| D、将混有HCl的Cl2通入饱和NaHCO3溶液中除去HCl |
下列关于碳酸钠和碳酸氢钠的比较中,正确的是( )
| A、二者在水中的溶解度不同,碳酸氢钠的溶解度大于碳酸钠的溶解度 |
| B、二者热稳定性不同,碳酸钠的热稳定性大于碳酸氢钠的热稳定性 |
| C、二者都能与盐酸反应放出二氧化碳气体,但产气量和反应快慢不同 |
| D、二者在一定的条件下可以相互转化 |
下列说法正确的是( )
| A、0.1mol/L NaHCO3溶液中:c(HCO3-)+c(CO32-)+c(OH-)>c(Na+)+c(H+)+c(H2CO3) |
| B、常温下,5mL 0.02mol/L HCl溶液与5mL 0.02mol/L Ba(OH)2溶液混合,经充分反应后,如果溶液体积为10mL,则溶液pH=12 |
| C、相同条件下pH=5的①NH4Cl溶液 ②CH3COOH溶液 ③稀盐酸,三种溶液中由水电离产生的c(H+):①>②>③ |
| D、常温下,将稀NaOH溶液与CH3COOH溶液混合,可能出现pH>7,且c(OH-)>c(Na+)>c(H+)>c(CH3COO-)的情况 |
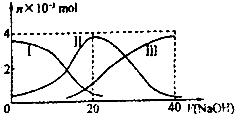 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量 变化如图(其中I代表H2A,Ⅱ代表HA-,Ⅲ代表A2-).根据图示判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量 变化如图(其中I代表H2A,Ⅱ代表HA-,Ⅲ代表A2-).根据图示判断,下列说法正确的是( )| A、当V(NaOH)=20mL时,溶液中离子浓度大小关系 c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
| B、等体积等浓度的NaOH溶液与H2A溶液混合后其溶液中水的电离程度比纯水大 |
| C、欲使NaHA溶液呈中性,可以向其中加入酸或碱 |
| D、向NaHA溶液加人水的过程中,pH可能增大也可能减小 |
已知在2L密闭容器内,发生:2NO(g)+O2(g)?2NO2(g),不能说明该反应已达到平衡状态的是( )
| A、容器内颜色保持不变 |
| B、v逆(NO)═2v正(O2) |
| C、单位时间内生成a mol的O2,同时生成2a mol NO2 |
| D、容器内密度保持不变 |
新航空燃油税从2012年2月14日开始征收,燃油税“燃”来好处之一节能减排,抑制燃油不合理消费.下列说法错误的是( )
| A、石油的裂解是生产乙烯的主要方法 |
| B、裂化汽油可以用于萃取溴水中的溴 |
| C、使用乙醇汽油,可以改善城市的空气质量 |
| D、石油在加热和催化剂作用下,可得到苯、甲苯等芳香烃 |